श्वसन इलेक्ट्रॉन परिवहन श्रृंखला में सुपरकॉम्प्लेक्स की उपस्थिति एससीएएफआई प्रोटीन द्वारा सुनिश्चित की जाती है। श्वसन श्रृंखला स्यूसिनिक एसिड के लिए कम इलेक्ट्रॉन परिवहन श्रृंखला
11.3.3.1. इलेक्ट्रॉन वाहक
इलेक्ट्रॉन वाहक सतह पर या आंतरिक माइटोकॉन्ड्रियल झिल्ली में गहराई में स्थित होते हैं, जो क्रॉस में व्यवस्थित होते हैं, जिनकी संख्या और पैकिंग घनत्व कोशिका की ऊर्जा आवश्यकताओं से संबंधित होता है।
कई इलेक्ट्रॉन वाहक प्रोटीन होते हैं जिनमें कृत्रिम समूह के रूप में हीम होता है।
हीम अणु के गुण उस प्रोटीन पर निर्भर करते हैं जिससे वह जुड़ा हुआ है। इसके अलावा, विभिन्न साइटोक्रोम में हेम्स साइड समूहों की संरचना और एपोप्रोटीन से जुड़ने की विधि में भिन्न हो सकते हैं। इसलिए, साइटोक्रोम रेडॉक्स क्षमता में भिन्न हो सकते हैं, हालांकि उन सभी में लगभग समान कृत्रिम समूह होते हैं।
इलेक्ट्रॉन वाहकों को साइटोक्रोम कहा जाता है क्योंकि वे लाल रंग के होते हैं। विभिन्न साइटोक्रोम को अक्षर सूचकांकों द्वारा निर्दिष्ट किया जाता है: एस 1, एस, ए, ए 3 -सर्किट में उनके स्थान के क्रम में।
एक अन्य प्रकार के गैर-हीम आयरन युक्त इलेक्ट्रॉन वाहक में प्रोटीन शामिल होते हैं जिनमें लोहे के परमाणु प्रोटीन सिस्टीन अवशेषों के सल्फहाइड्रील समूहों के साथ-साथ अवशेषों के सल्फहाइड्रील आयनों से जुड़े होते हैं, जिससे आयरन-सल्फर कॉम्प्लेक्स या केंद्र बनते हैं ( चित्र 29)।

चावल। 29.लौह-सल्फर केंद्र की संरचना
साइटोक्रोम की तरह, ऐसे केंद्रों में लोहे के परमाणु इलेक्ट्रॉनों को स्वीकार और दान कर सकते हैं, बारी-बारी से फेरो (Fe 2+) और फेरी (Fe 3+) अवस्था में जा सकते हैं। आयरन-सल्फर केंद्र फ्लेविन युक्त एंजाइमों के साथ मिलकर कार्य करते हैं, जो वसा ऑक्सीकरण में शामिल सक्सेनेट डिहाइड्रोजनेज और डिहाइड्रोजनेज से इलेक्ट्रॉनों को स्वीकार करते हैं।
एक अन्य प्रकार का ट्रांसपोर्टर एफएमएन युक्त प्रोटीन है। एफएमएन (फ्लेविन एडेनिन मोनोन्यूक्लियोटाइड) एक यौगिक है जो एफएडी अणु का फ्लेविन आधा है। एफएमएन इलेक्ट्रॉनों को एफएडीएन से लौह-सल्फर केंद्रों में स्थानांतरित करता है।
सभी प्रोटीन वाहक अभिन्न प्रोटीन होते हैं जो झिल्ली में एक निश्चित स्थिति पर कब्जा कर लेते हैं और एक निश्चित तरीके से उन्मुख होते हैं। अपवाद साइटोक्रोम सी है, जो बाहरी झिल्ली से शिथिल रूप से बंधा होता है और आसानी से इसे छोड़ देता है।

एकमात्र गैर-प्रोटीन इलेक्ट्रॉन वाहक यूबिकिनोन है, इसे यह नाम इसलिए दिया गया है क्योंकि, एक तरफ, यह एक क्विनोन है, और दूसरी तरफ, यह हर जगह (अंग्रेजी से) पाया जाता है। देशव्यापी- सर्वव्यापी)। इसका संक्षिप्त नाम CoQ, UQ या केवल Q है। सभी लौह-सल्फर केंद्र यूबिकिनोन को इलेक्ट्रॉन दान करते हैं।
कमी के दौरान, यूबिकिनोन न केवल इलेक्ट्रॉन, बल्कि प्रोटॉन भी प्राप्त करता है (चित्र 30)।

चित्र.30.यूबिकिनोन - कोएंजाइम क्यू (ए)
और इसके रेडॉक्स परिवर्तन (बी)
एक-इलेक्ट्रॉन कमी के साथ यह सेमीक्विनोन (एक कार्बनिक मुक्त कण) में बदल जाता है, और दो-इलेक्ट्रॉन कमी के साथ यह हाइड्रोक्विनोन में बदल जाता है। यह एक मुक्त रेडिकल का मध्यवर्ती गठन है जो यूबिकिनोन को दो नहीं, बल्कि एक इलेक्ट्रॉन के वाहक के रूप में कार्य करने की अनुमति देता है। बहुत लंबी हाइड्रोफोबिक पूंछ (लगातार दस आइसोप्रेनॉइड अवशेषों में 40 कार्बन परमाणु) यूबिकिनोन को आंतरिक माइटोकॉन्ड्रियल झिल्ली की गैर-ध्रुवीय परत में आसानी से डालने और स्वतंत्र रूप से स्थानांतरित करने की क्षमता देती है।
11.3.3.2. वैक्टर का स्थान
वाहकों के बीच इलेक्ट्रॉनों का प्रवाह उच्च कमी क्षमता (यानी, कम रेडॉक्स क्षमता) वाले वाहक से कम कमी क्षमता (यानी, अधिक ऑक्सीकृत, उच्च रेडॉक्स क्षमता वाले) वाले वाहक की ओर निर्देशित होता है (चित्र 31)।

चित्र.31.माइटोकॉन्ड्रिया में श्वसन श्रृंखला घटकों की रेडॉक्स क्षमता
माइटोकॉन्ड्रियल श्रृंखला में, ट्रांसपोर्टरों के पास अलग-अलग रेडॉक्स क्षमताएं होती हैं।
श्रृंखला में इलेक्ट्रॉन वाहक सर्किट में ऐसे स्थित होते हैं कि डीजी 0 (मुक्त ऊर्जा) धीरे-धीरे कम हो जाती है और रेडॉक्स क्षमता तदनुसार बढ़ जाती है। श्रृंखला से सटे वाहक में इलेक्ट्रॉन स्थानांतरण के प्रत्येक चरण में, मुक्त ऊर्जा जारी होती है।
ग्लूकोज के ऑक्सीकरण के दौरान, इलेक्ट्रॉनों को NADH और FADH 2 से ऑक्सीजन में स्थानांतरित किया जाता है। कई ट्रांसपोर्टर इस प्रक्रिया में शामिल होते हैं, लेकिन उन्हें चार परिसरों में बांटा जा सकता है जो माइटोकॉन्ड्रियल झिल्ली में अंतर्निहित होते हैं
(चित्र 32)।

चावल। 32.चार इलेक्ट्रॉन परिवहन परिसर
माइटोकॉन्ड्रियल झिल्ली में
कॉम्प्लेक्स के बीच, इलेक्ट्रॉन मोबाइल वाहक के साथ एक साथ चलते हैं: यूबिकिनोन और साइटोक्रोम सी। यूबिकिनोन कॉम्प्लेक्स I और II से इलेक्ट्रॉन प्राप्त करता है और उन्हें कॉम्प्लेक्स III में स्थानांतरित करता है। साइटोक्रोम c कॉम्प्लेक्स III और IV के बीच मध्यस्थ के रूप में कार्य करता है। कॉम्प्लेक्स I इलेक्ट्रॉनों को NADH से Q में स्थानांतरित करता है; कॉम्प्लेक्स II - सक्सिनेट से FADN 2 से Q तक; कॉम्प्लेक्स III साइटोक्रोम सी को कम करने के लिए QH 2 का उपयोग करता है, और कॉम्प्लेक्स IV साइटोक्रोम से इलेक्ट्रॉनों को स्थानांतरित करता है साथऑक्सीजन के लिए. कॉम्प्लेक्स I, III और IV को क्रमशः NADH-CoQ रिडक्टेस, CoQH 2-साइटोक्रोम कहा जाता है साथ-रिडक्टेस और साइटोक्रोम ऑक्सीडेज। कॉम्प्लेक्स IV - साइटोक्रोम ऑक्सीडेज - में कई प्रोटीन होते हैं। यह साइटोक्रोम से इलेक्ट्रॉन प्राप्त करता है साथआंतरिक माइटोकॉन्ड्रियल झिल्ली के बाहर। ऑक्सीजन के रास्ते में, ये इलेक्ट्रॉन साइटोक्रोम से होकर गुजरते हैं एऔर एक 3, जिसमें तांबे के परमाणु होते हैं, जो बारी-बारी से Cu + और Cu 2+ अवस्था में परिवर्तित हो जाते हैं। साइटोक्रोम ऑक्सीडेज मुक्त ऑक्सीजन को कम करता है:
ओ 2+4 ई - + 4H + ® 2H 2 O
11.3.3.3. मिशेल का रसायनपरासरण सिद्धांत
श्वसन श्रृंखला के साथ इलेक्ट्रॉनों के परिवहन से एटीपी का उत्पादन होता है। एटीपी संश्लेषण के साथ इलेक्ट्रॉन परिवहन को युग्मित करने के तंत्र की अवधारणा 1961 में अंग्रेजी बायोकेमिस्ट पीटर मिशेल द्वारा विकसित की गई थी (मिशेल को 1978 में नोबेल पुरस्कार से सम्मानित किया गया था)। मिशेल ने पाया कि इलेक्ट्रॉनों के प्रवाह के कारण प्रोटॉन को माइटोकॉन्ड्रिया से आसपास के वातावरण में पंप किया जाता है, जिससे झिल्ली में एक प्रोटॉन ग्रेडिएंट बनता है (बाहरी समाधान का पीएच कम हो जाता है)। चूँकि प्रोटॉन धनात्मक रूप से आवेशित कण होते हैं, माइटोकॉन्ड्रिया से उनके पंपिंग के कारण, झिल्ली पर विद्युत क्षमता में अंतर (माइनस - अंदर) और पीएच अंतर (अधिक - अंदर) उत्पन्न होता है। साथ में, विद्युत और एकाग्रता प्रवणताएं (मिशेल के अनुसार) प्रोटॉन प्रेरक बल का निर्माण करती हैं, जो एटीपी के संश्लेषण के लिए ऊर्जा का स्रोत है (चित्र 33)।


चावल। 33.आंतरिक में एटीपी संश्लेषण की योजना
माइटोकॉन्ड्रियल झिल्ली
प्रोटॉन प्रेरक बल एटीपी सिंथेज़ कॉम्प्लेक्स को संचालित करता है, जो एडीपी और फॉस्फोरस से एटीपी को संश्लेषित करने के लिए इलेक्ट्रॉनों के प्रवाह का उपयोग करता है। कॉम्प्लेक्स विशेष प्रोटॉन चैनल (मशरूम के आकार के प्रक्षेपण जो क्राइस्टे की आंतरिक सतह को कवर करते हैं) हैं। कॉम्प्लेक्स को दो परस्पर जुड़े घटकों F 0 F 1 द्वारा दर्शाया गया है, जिनमें से प्रत्येक में कई प्रोटीन अणु होते हैं। F 0 झिल्ली में धँसा हुआ है, और F 1 इसकी सतह पर स्थित है। यह F1 में है कि ATP संश्लेषित होता है, जबकि F0 प्रोटॉन चैनल का कार्य स्वयं करता है (चित्र 34)।

चित्र 34.ई. कोलाई से एफ 0 एफ 1 एटीपी सिंथेटेज़ की "मशरूम" संरचना का योजनाबद्ध प्रतिनिधित्व। F 0 घटक झिल्ली में प्रवेश करता है, प्रोटॉन के लिए एक चैनल बनाता है। यह माना जाता है कि एफ 1 में तीन ए और तीन बी सबयूनिट होते हैं, जिन्हें इस तरह व्यवस्थित किया जाता है कि वे "मशरूम कैप" की तरह एक हेक्सामेरिक संरचना बनाते हैं, और एक जी, एक डी और एक ई सबयूनिट होते हैं, जो एफ 0 को जोड़ने वाली एक "रॉड" बनाते हैं। एफ 1 चैनल के लिए
यह ठीक से ज्ञात नहीं है कि एटीपी सिंथेटेज़ के माध्यम से एटीपी कैसे उत्पन्न होता है। एक सिद्धांत के अनुसार, F0 कारक के माध्यम से प्रोटॉन के स्थानांतरण के दौरान, F1 घटक में गठनात्मक परिवर्तन होते हैं, जो ADP और फास्फोरस से ATP को संश्लेषित करता है।
एनएडीएच से ऑक्सीजन में स्थानांतरित इलेक्ट्रॉनों की प्रत्येक जोड़ी के लिए, माइटोकॉन्ड्रियल मैट्रिक्स से 10 प्रोटॉन पंप किए जाते हैं। इस प्रकार, 1 एनएडीएच अणु के ऑक्सीकरण से 2.5 एटीपी अणुओं का संश्लेषण होता है, और 1 एफएडीएच 2 अणु के ऑक्सीकरण से 1.5 एटीपी अणुओं का संश्लेषण होता है। पहले, यह माना जाता था कि क्रमशः तीन और दो एटीपी अणुओं को संश्लेषित किया गया था। इन मात्राओं को आमतौर पर पी/ओ अनुपात कहा जाता है, क्योंकि 2 इलेक्ट्रॉनों का स्थानांतरण 1 ऑक्सीजन परमाणु की कमी के बराबर है।
ग्लूकोज अणु के सीओ 2 और एच 2 ओ में ऑक्सीकरण के दौरान एटीपी की उपज।
ग्लाइकोलाइसिस 2 एटीपी अणुओं का उत्पादन करता है (4 का उत्पादन होता है, लेकिन 2 का उपभोग होता है)। ग्लाइकोलाइसिस के दौरान, साइटोप्लाज्म में ग्लूकोज के प्रति 1 अणु में NADH के 2 अणु भी बनते हैं। साइट्रिक एसिड चक्र में 2 एटीपी अणु बनते हैं (1 ग्लूकोज अणु से 2 एसिटाइल-सीओए अणु बनते हैं, जिससे चक्र के दो मोड़ शुरू होते हैं)।
ग्लूकोज के प्रत्येक 1 अणु के लिए, पाइरूवेट डिहाइड्रोजनेज NADH के 2 अणु पैदा करता है, और साइट्रिक एसिड चक्र NADH के 6 अणु पैदा करता है। उनके ऑक्सीकरण से 20 एटीपी अणुओं का संश्लेषण होता है। सक्सेनेट के फ्यूमरेट में रूपांतरण के दौरान FADH 2 के ऑक्सीकरण के कारण तीन और एटीपी अणु बनते हैं।
एटीपी अणुओं का कुल उत्पादन इस बात पर निर्भर करेगा कि श्वसन श्रृंखला में एनएडीएच पहुंचाने के लिए कोशिकाओं द्वारा किस शटल तंत्र (ग्लिसरोफॉस्फेट और मैलेट एस्पार्टेट) का उपयोग किया जाता है। ग्लिसरॉल फॉस्फेट तंत्र में, एनएडीएच से इलेक्ट्रॉनों को ग्लिसरॉल-3-फॉस्फेट बनाने के लिए डायहाइड्रॉक्सीएसीटोन फॉस्फेट में स्थानांतरित किया जाता है, जो इलेक्ट्रॉनों को श्वसन श्रृंखला में स्थानांतरित करता है (चित्र 35)। यह एंजाइम ग्लिसरॉल-3-फॉस्फेट डिहाइड्रोजनेज की भागीदारी से होता है। साइटोप्लाज्मिक एनएडीएच की मदद से, माइटोकॉन्ड्रियल एफएडी, जो फ्लेवोप्रोटीन - ग्लिसरॉल-3-फॉस्फेट डिहाइड्रोजनेज का एक कृत्रिम समूह है, को बहाल किया जाता है।

चावल। 35.ग्लिसरॉल फॉस्फेट शटल तंत्र
एक अन्य शटल प्रणाली, मैलेट-एस्पार्टेट प्रणाली, इलेक्ट्रॉनों को साइटोप्लाज्मिक एनएडीएच से माइटोकॉन्ड्रियल एनएडी + में स्थानांतरित करती है (चित्र 36)। इससे माइटोकॉन्ड्रियल एनएडीएच का निर्माण होता है, जो आगे चलकर इलेक्ट्रॉन परिवहन श्रृंखला में ऑक्सीकृत हो जाता है। साइटोप्लाज्म में, NADH ऑक्सालोएसीटेट को मैलेट में कम कर देता है। उत्तरार्द्ध, एक वाहक की मदद से, माइटोकॉन्ड्रिया में प्रवेश करता है, जहां इसे एनएडी + की कमी के साथ ऑक्सालोएसीटेट में पुन: ऑक्सीकृत किया जाता है। ऑक्सालोएसीटेट स्वयं माइटोकॉन्ड्रिया को नहीं छोड़ सकता है, इसलिए यह पहले एस्पार्टेट में बदल जाता है, जिसे वाहक द्वारा साइटोप्लाज्म में ले जाया जाता है। साइटोप्लाज्म में, एस्पार्टेट डीमिनेट हो जाता है, ऑक्सालोएसीटेट में बदल जाता है और इस तरह शटल तंत्र बंद हो जाता है।

चित्र.36.इलेक्ट्रॉन स्थानांतरण के लिए मैलेट-एस्पार्टेट शटल प्रणाली
ये प्रोटीन कॉम्प्लेक्स और इलेक्ट्रॉन वाहक हैं जो माइटोकॉन्ड्रिया की आंतरिक झिल्ली पर तैरते हैं, श्रृंखला के साथ इलेक्ट्रॉनों को एक दूसरे में स्थानांतरित करते हैं और इस तरह ऊर्जा उत्पन्न करते हैं। चार श्वसन प्रोटीन कॉम्प्लेक्स हैं, और यह अभी भी स्पष्ट नहीं है कि वे झिल्ली पर कैसे व्यवस्थित होते हैं: क्या वे एक-दूसरे से स्वतंत्र रूप से तैरते हैं या एक साथ जुड़ते हैं, तथाकथित सुपरकॉम्प्लेक्स बनाते हैं। स्पैनिश शोधकर्ताओं के एक समूह ने पाया कि एससीएएफआई (सुपरकॉम्प्लेक्स असेंबली फैक्टर I) नामक एक प्रोटीन विशेष रूप से श्वसन परिसरों के संयोजन को सुपरकॉम्प्लेक्स में नियंत्रित करता है।
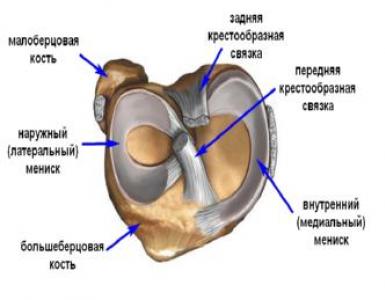
कई दशक पहले, जब माइटोकॉन्ड्रिया के श्वसन प्रोटीन परिसरों को अलग किया गया था और उनका अध्ययन किया गया था, तो यह माना गया था कि वे एक दूसरे से स्वतंत्र रूप से झिल्ली में मौजूद हैं और केवल उनके बीच यात्रा करने वाले इलेक्ट्रॉन वाहक - यूबिकिनोन और साइटोक्रोम सी (छवि) की मदद से संचार करते हैं। 1). इस धारणा को "द्रव मॉडल" कहा जाता है। हालाँकि, धीरे-धीरे सबूत सामने आए कि स्थिति इतनी सरल नहीं है और श्वसन परिसरों को आपस में बड़ी संरचनाओं - "सुपरकॉम्प्लेक्स" में एकजुट किया जा सकता है।
उदाहरण के लिए, यह पाया गया कि कॉम्प्लेक्स I आमतौर पर कॉम्प्लेक्स III या IV की अनुपस्थिति में अस्थिर होता है। और 2000 में, एक साहसिक परिकल्पना सामने रखी गई - इसे "सॉलिड मॉडल" कहा गया - जिसके अनुसार कॉम्प्लेक्स I, III और IV को एक साथ एक विशाल सुपरकॉम्प्लेक्स में संयोजित किया जाता है जिसे रेस्पिरसोम कहा जाता है, जिसके परिणामस्वरूप वे अधिक सामंजस्यपूर्ण रूप से काम करते हैं ( हरमन शेग्गर, कैथी फ़िफ़र, 2000 देखें। यीस्ट और स्तनधारी माइटोकॉन्ड्रिया की श्वसन श्रृंखलाओं में सुपरकॉम्प्लेक्स)। आवश्यक श्वसन को गोजातीय हृदय की मांसपेशी के माइटोकॉन्ड्रिया से अलग कर दिया गया था, लेकिन, हमेशा की तरह ऐसे नाजुक आणविक अध्ययनों में, यह संभावना बनी रही कि यह केवल एक गलत तरीके से चयनित तकनीक का एक आर्टिफैक्ट था, और कॉम्प्लेक्स गोजातीय माइटोकॉन्ड्रियल में नहीं बल्कि एक साथ जुड़े हुए थे। झिल्ली, लेकिन सीधे शोधकर्ता की टेस्ट ट्यूब में। बाद के वर्षों में, रेस्पिरेसोम के अस्तित्व को साबित करने या अस्वीकृत करने के लिए कई प्रयास किए गए, लेकिन व्यर्थ: रेस्पिरेसोम के पक्ष या विपक्ष में कोई निर्णायक तर्क प्राप्त नहीं हुआ। कुछ प्रोटीन अलगाव तकनीकों का उपयोग करके माइटोकॉन्ड्रिया में रेस्पिरैसोम और अन्य सुपरकॉम्प्लेक्स का पूरी तरह से पता लगाया जा सकता था, लेकिन यह अभी भी स्पष्ट नहीं था कि यह एक तथ्य था या एक कलाकृति।
चर्चा किए गए कार्य के लेखकों ने समस्या को एक अलग कोण से देखने का निर्णय लिया। यदि रेस्पिरैसोम्स (और अन्य सुपरकॉम्प्लेक्स) एक कलाकृति नहीं हैं, तो संभवतः उनमें न केवल श्वसन कॉम्प्लेक्स शामिल होंगे, बल्कि कुछ अन्य सहायक प्रोटीन भी होंगे। और यदि इन सहायक प्रोटीनों की पहचान की जाती है और फिर उनके साथ "खेला" जाता है - उदाहरण के लिए, उन्हें बंद या चालू करना - तो आप सुपरकॉम्प्लेक्स के अस्तित्व के अप्रत्यक्ष साक्ष्य (या, इसके विपरीत, खंडन) प्राप्त कर सकते हैं, और आम तौर पर यह भी समझ सकते हैं कि किन परिस्थितियों में ये कॉम्प्लेक्स बनते हैं और इनकी आवश्यकता क्यों है?
इसलिए, शोधकर्ताओं ने पहले माइटोकॉन्ड्रिया से व्यक्तिगत रूप से सुपरकॉम्प्लेक्स और श्वसन कॉम्प्लेक्स को अलग किया (यह नीले देशी इलेक्ट्रोफोरेसिस का उपयोग करके किया गया था (बीएन-पेज देखें) - प्रोटीन मिश्रण को अलग करने के सबसे सौम्य तरीकों में से एक), और फिर उन प्रोटीनों का विश्लेषण किया जो सुपर कॉम्प्लेक्स बनाते हैं और "एकल" कॉम्प्लेक्स। "श्वसन कॉम्प्लेक्स।
और यह पता चला कि एक प्रोटीन (जिसका अस्पष्ट नाम Cox7a2l है - साइटोक्रोम सी ऑक्सीडेज सबयूनिट VIIa पॉलीपेप्टाइड 2-लाइक) केवल श्वसन कॉम्प्लेक्स IV वाले सुपर कॉम्प्लेक्स में मौजूद है (अर्थात, श्वसन और सुपर कॉम्प्लेक्स III + IV में), और है एकल कॉम्प्लेक्स में नहीं पाया गया। समानांतर में, शोधकर्ता इतने भाग्यशाली थे कि उन्हें गलती से पता चला कि इस प्रोटीन के क्षतिग्रस्त (और स्पष्ट रूप से गैर-व्यवहार्य) रूप के साथ तीन उत्परिवर्ती माउस सेल लाइनों में, माइटोकॉन्ड्रियल झिल्ली में जटिल IV से जुड़े सुपरकॉम्प्लेक्स का बिल्कुल भी पता नहीं चला था। इसके अलावा, यदि सामान्य प्रोटीन के लिए एक जीन उत्परिवर्ती कोशिकाओं में डाला जाता है, तो उनमें ये सुपरकॉम्प्लेक्स बनने लगते हैं। इस सब से, शोधकर्ताओं ने एक तार्किक निष्कर्ष निकाला: यह प्रोटीन जटिल IV को सुपरकॉम्प्लेक्स बनाने में मदद करता है और इसलिए इसका नाम बदलकर सुपरकॉम्प्लेक्स असेंबली फैक्टर I (एससीएएफआई) रखा जाना चाहिए और अधिक विस्तार से अध्ययन किया जाना चाहिए।
निष्पक्ष होने के लिए, हम ध्यान दें कि सुपरकॉम्प्लेक्स को स्थिर करने वाले प्रोटीन का विचार नया नहीं है: पिछले साल, दो प्रोटीन, आरसीएफ 1 और आरसीएफ 2, पहले से ही खमीर में खोजे गए थे, जो सुपर कॉम्प्लेक्स के निर्माण में भी शामिल थे (देखें: वी. स्ट्रोगोलोवा) एट अल., 2012. आरसीएफ1 और आरसीएफ2, हाइपोक्सिया-प्रेरित जीन 1 प्रोटीन परिवार के सदस्य, माइटोकॉन्ड्रियल साइटोक्रोम बीसी1-साइटोक्रोम सी ऑक्सीडेज सुपरकॉम्प्लेक्स के महत्वपूर्ण घटक हैं)।
सुपर कॉम्प्लेक्स का निर्माण क्यों आवश्यक है? शोधकर्ताओं ने इस घटना के लिए एक सुंदर स्पष्टीकरण प्रस्तावित किया (चित्र 2)।
मान लीजिए कि झिल्ली में कोई सुपरकॉम्प्लेक्स नहीं हैं, और श्वसन कॉम्प्लेक्स व्यक्तिगत रूप से और एक दूसरे से स्वतंत्र रूप से काम करते हैं। फिर इलेक्ट्रॉनों का स्थानांतरण केवल एक शाखा के साथ एक सरल मार्ग से होता है: कॉम्प्लेक्स I इलेक्ट्रॉनों को NADH से कोएंजाइम Q में स्थानांतरित करता है (आइए हम इस कोएंजाइम Q के पूल को "CoQ NADH" कहते हैं), कॉम्प्लेक्स II इलेक्ट्रॉनों को सक्सिनेट से कोएंजाइम Q में स्थानांतरित करता है (हम' हम कोएंजाइम Q के इस पूल को "CoQ FAD" कहेंगे, क्योंकि कॉम्प्लेक्स II में ऑक्सीकरण सहकारक FAD की मदद से होता है); इसके बाद, कोएंजाइम क्यू के दोनों पूलों से, कॉम्प्लेक्स III का उपयोग करके इलेक्ट्रॉनों को साइटोक्रोम सी में स्थानांतरित किया जाता है (अर्थात, साइटोक्रोम सी का केवल एक बड़ा पूल बनता है, चलो इसे साइट सी दोनों कहते हैं, क्योंकि यह दोनों धाराओं से संबंधित है); और अंत में, साइटोक्रोम सी, कॉम्प्लेक्स IV द्वारा फंसा हुआ, इलेक्ट्रॉनों को ऑक्सीजन में स्थानांतरित करता है। दूसरे शब्दों में, पूरे सिस्टम में IV कॉम्प्लेक्स का केवल एक पूल है - आइए इसे IV दोनों कहें।
यदि, एकाकी संकुलों के अलावा, झिल्ली में तैरते हुए सुपरकॉम्प्लेक्स भी हों, तो इलेक्ट्रॉन मार्ग अधिक जटिल और शाखित होता है। मुक्त कॉम्प्लेक्स के माध्यम से ऊपर वर्णित मार्ग के अलावा, वे श्वसन में भी प्रवेश कर सकते हैं, जहां अंततः कॉम्प्लेक्स IV का एक अलग पूल (आइए इसे IV NADH कहते हैं) उन्हें साइटोक्रोम सी के एक अलग पूल से ऑक्सीजन में स्थानांतरित करता है। कॉम्प्लेक्स II की मदद से, वे सुपरकॉम्प्लेक्स III+IV तक पहुंच सकते हैं, जहां से, फिर से, वे ऑक्सीजन में जाएंगे (हम कॉम्प्लेक्स के इस पूल को IV IV FAD कहेंगे)। इस प्रकार, हमारे पास कॉम्प्लेक्स IV के तीन पूल हैं - IV NADH, IV FAD और IV दोनों।
इस विभाजन के परिणामस्वरूप, सिस्टम अधिक लचीला हो जाता है, एक सब्सट्रेट के साथ अतिसंतृप्ति और सब्सट्रेट्स के बीच प्रतिस्पर्धा के खिलाफ बीमा हो जाता है और, इसके विपरीत, इष्टतम स्तरों पर विभिन्न सब्सट्रेट्स के उपयोग के लिए अनुकूलित हो जाता है। उदाहरण के लिए, यदि आप माइटोकॉन्ड्रिया को विशेष रूप से सक्सिनेट (जो एफएडी मार्ग के साथ इलेक्ट्रॉनों को भेजता है) के साथ "फ़ीड" करते हैं, तो सुपरकॉम्प्लेक्स की अनुपस्थिति में वे इसे अपनी उपस्थिति की तुलना में तेजी से संसाधित करेंगे। हालाँकि, यदि इन माइटोकॉन्ड्रिया को सक्सिनेट और पाइरूवेट + मैलेट (एनएडीएच मार्ग के माध्यम से इलेक्ट्रॉनों को भेजना) वाले माध्यम में रखा जाता है, तो सुपरकॉम्प्लेक्स वाले माइटोकॉन्ड्रिया में सक्सेनेट की प्रक्रिया नहीं बदलेगी, लेकिन सुपरकॉम्प्लेक्स के बिना माइटोकॉन्ड्रिया में यह काफी कम हो जाएगा (चित्र) .3 ).

जाहिरा तौर पर, इलेक्ट्रॉन परिवहन श्रृंखला में सुपरकॉम्प्लेक्स की उपस्थिति बस एक अतिरिक्त और वैकल्पिक "धनुष" है। हालाँकि सुपरकॉम्प्लेक्स स्पष्ट रूप से इस श्रृंखला में एर्गोनॉमिक्स जोड़ते हैं, यहां तक कि उनकी अनुपस्थिति में भी माइटोकॉन्ड्रिया (साथ ही वे जानवर जिनमें ये माइटोकॉन्ड्रिया काम करते हैं) बहुत अच्छा महसूस करते हैं। चर्चा के तहत कार्य, सबसे पहले, सुपरकॉम्प्लेक्स की उपस्थिति के लिए आनुवंशिक प्रमाण प्रदान करता है, और दूसरा, इलेक्ट्रॉन परिवहन श्रृंखला की प्लास्टिसिटी का एक सुंदर सिद्धांत प्रस्तावित करता है।
प्रोटॉन विभव कहाँ प्रेरित होता है? प्रोटॉन क्षमता को एटीपी सिंथेज़ द्वारा एटीपी की रासायनिक बंधन ऊर्जा में परिवर्तित किया जाता है। ईटीसी और एटीपी सिंथेज़ के संयुग्म कार्य को ऑक्सीडेटिव फॉस्फोराइलेशन कहा जाता है।
यूकेरियोटिक माइटोकॉन्ड्रिया में, इलेक्ट्रॉन परिवहन श्रृंखला NADH के ऑक्सीकरण और कॉम्प्लेक्स I द्वारा यूबिकिनोन Q की कमी के साथ शुरू होती है। इसके बाद, कॉम्प्लेक्स II सक्सिनेट को फ्यूमरेट में ऑक्सीकरण करता है और यूबिकिनोन Q को कम करता है। यूबिकिनोन क्यू को साइटोक्रोम सी कॉम्प्लेक्स III द्वारा ऑक्सीकरण और कम किया जाता है। श्रृंखला के अंत में, कॉम्प्लेक्स IV पानी बनाने के लिए साइटोक्रोम सी से ऑक्सीजन तक इलेक्ट्रॉनों के स्थानांतरण को उत्प्रेरित करता है। प्रतिक्रिया के परिणामस्वरूप, प्रत्येक पारंपरिक रूप से जारी 6 प्रोटॉन और 6 इलेक्ट्रॉनों के लिए, O2 के 1 अणु और NAD∙H के 10 अणुओं के व्यय के कारण पानी के 2 अणु निकलते हैं।
कॉम्प्लेक्स I या NADH डिहाइड्रोजनेज कॉम्प्लेक्स NAD-H को ऑक्सीकृत करता है। यह कॉम्प्लेक्स सेलुलर श्वसन की प्रक्रियाओं में एक केंद्रीय भूमिका निभाता है। एटीपी संश्लेषण के लिए लगभग 40% प्रोटॉन ग्रेडिएंट इस कॉम्प्लेक्स द्वारा निर्मित होता है। कॉम्प्लेक्स I NADH को ऑक्सीकृत करता है और यूबिकिनोन के एक अणु को कम करता है, जो झिल्ली में जारी होता है। प्रत्येक NADH अणु के ऑक्सीकरण के लिए, कॉम्प्लेक्स चार प्रोटॉन को झिल्ली में स्थानांतरित करता है। एनएडीएच डिहाइड्रोजनेज कॉम्प्लेक्स इसमें से दो इलेक्ट्रॉन लेता है और उन्हें यूबिकिनोन में स्थानांतरित करता है। यूबिकिनोन लिपिड घुलनशील है। झिल्ली के अंदर यूबिकिनोन जटिल III तक फैल जाता है। उसी समय, कॉम्प्लेक्स I मैट्रिक्स से 2 प्रोटॉन और 2 इलेक्ट्रॉनों को माइटोकॉन्ड्रिया में पंप करता है।
जटिल I की इलेक्ट्रॉन परिवहन श्रृंखला। ग्रे तीर - असंभावित या अब निष्क्रिय परिवहन मार्ग
N5 क्लस्टर की क्षमता बहुत कम है और यह पूरी श्रृंखला में इलेक्ट्रॉनों के कुल प्रवाह की दर को सीमित करता है। लौह-सल्फर केंद्रों (चार सिस्टीन अवशेष) के लिए सामान्य लिगैंड के बजाय, यह तीन सिस्टीन अवशेषों और एक हिस्टिडीन अवशेष द्वारा समन्वित होता है, और आवेशित ध्रुवीय अवशेषों से भी घिरा होता है, हालांकि यह एंजाइम में गहराई से स्थित होता है।
क्लस्टर N7 केवल कुछ बैक्टीरिया के कॉम्प्लेक्स I में मौजूद होता है। यह अन्य समूहों से काफी दूर है और उनके साथ इलेक्ट्रॉनों का आदान-प्रदान नहीं कर सकता है, इसलिए यह स्पष्ट रूप से एक अवशेष है। कॉम्प्लेक्स I से संबंधित कुछ जीवाणु परिसरों में, N7 और अन्य समूहों के बीच चार संरक्षित सिस्टीन अवशेष पाए गए, और जीवाणु परिसर I में एक्विफ़ेक्स एओलिकस N7 को शेष समूहों से जोड़ने वाले एक अतिरिक्त Fe 4 S 4 क्लस्टर की खोज की गई। इससे यह निष्कर्ष निकलता है ए. एओलिकसकॉम्प्लेक्स I, NADH के अलावा, एक अन्य इलेक्ट्रॉन दाता का उपयोग कर सकता है, जो उन्हें N7 के माध्यम से स्थानांतरित करता है।
एनएडीएच डिहाइड्रोजनेज कॉम्प्लेक्स ट्राइकारबॉक्सिलिक एसिड चक्र के दौरान मैट्रिक्स में गठित एनएडीएच को ऑक्सीकरण करता है। एनएडीएच से इलेक्ट्रॉनों का उपयोग झिल्ली ट्रांसपोर्टर, यूबिकिनोन क्यू को बहाल करने के लिए किया जाता है, जो उन्हें माइटोकॉन्ड्रियल इलेक्ट्रॉन परिवहन श्रृंखला के अगले कॉम्प्लेक्स, कॉम्प्लेक्स III या साइटोक्रोम में स्थानांतरित करता है। ईसा पूर्व 1-जटिल.
एनएडीएच डिहाइड्रोजनेज कॉम्प्लेक्स एक प्रोटॉन पंप की तरह काम करता है: प्रत्येक ऑक्सीकृत एनएडीएच और कम क्यू के लिए, चार प्रोटॉन को झिल्ली के माध्यम से इंटरमेम्ब्रेन स्पेस में पंप किया जाता है:
प्रतिक्रिया के दौरान उत्पन्न विद्युत रासायनिक क्षमता का उपयोग एटीपी को संश्लेषित करने के लिए किया जाता है। कॉम्प्लेक्स I द्वारा उत्प्रेरित प्रतिक्रिया प्रतिवर्ती है, एक प्रक्रिया जिसे एरोबिक सक्सिनेट-प्रेरित NAD+ कमी कहा जाता है। उच्च झिल्ली क्षमता और अतिरिक्त कम यूबिकिनोल्स की स्थितियों के तहत, कॉम्प्लेक्स अपने इलेक्ट्रॉनों का उपयोग करके एनएडी+ को कम कर सकता है और प्रोटॉन को मैट्रिक्स में वापस भेज सकता है। यह घटना आमतौर पर तब होती है जब सक्सेनेट बहुत अधिक होता है लेकिन ऑक्सालोएसीटेट या मैलेट कम होता है। यूबिकिनोन की कमी एंजाइम सक्सेनेट डिहाइड्रोजनेज या माइटोकॉन्ड्रियल द्वारा की जाती है। एक उच्च प्रोटॉन ग्रेडिएंट की स्थितियों के तहत, यूबिकिनोल के लिए कॉम्प्लेक्स की आत्मीयता बढ़ जाती है, और इसकी एकाग्रता में वृद्धि के कारण यूबिकिनोल की रेडॉक्स क्षमता कम हो जाती है, जिससे आंतरिक माइटोकॉन्ड्रियल झिल्ली की विद्युत क्षमता के साथ इलेक्ट्रॉनों का रिवर्स परिवहन संभव हो जाता है। एनएडी. यह घटना प्रयोगशाला स्थितियों में देखी गई थी, लेकिन यह अज्ञात है कि यह जीवित कोशिका में होती है या नहीं।
कॉम्प्लेक्स I में अनुसंधान के शुरुआती चरणों के दौरान, एक व्यापक रूप से चर्चा किया गया मॉडल इस धारणा पर आधारित था कि कॉम्प्लेक्स में एक समान प्रणाली संचालित होती है। हालाँकि, बाद के अध्ययनों में कॉम्प्लेक्स I में कोई आंतरिक रूप से बाध्य क्विनोन नहीं पाया गया और इस परिकल्पना को पूरी तरह से खारिज कर दिया गया।
ऐसा प्रतीत होता है कि एनएडीएच डिहाइड्रोजनेज कॉम्प्लेक्स में एंजाइम में परिवर्तन के माध्यम से एक अद्वितीय प्रोटॉन परिवहन तंत्र है। ND2, ND4 और ND5 सबयूनिट को एंटीपोर्ट-लाइक कहा जाता है क्योंकि वे एक-दूसरे और बैक्टीरियल एमआरपी Na + /H + एंटीपोर्ट के समरूप हैं। ये तीन उपइकाइयाँ तीन प्रमुख प्रोटॉन चैनल बनाती हैं, जो संरक्षित आवेशित अमीनो एसिड अवशेषों (मुख्य रूप से लाइसिन और ग्लूटामेट) से बने होते हैं। चौथा प्रोटॉन चैनल Nqo8 सबयूनिट और छोटे सबयूनिट ND6, ND4L और ND3 के भाग से बनता है। चैनल संरचना में एंटीपोर्ट-जैसे सबयूनिट्स के समान चैनलों के समान है, लेकिन इसमें मैट्रिक्स पक्ष पर असामान्य रूप से बड़ी संख्या में घनी पैक ग्लूटामेट अवशेष होते हैं, यही कारण है कि इसे ई-चैनल कहा जाता है (लैटिन ई को मानक के रूप में उपयोग किया जाता है) ग्लूटामेट के लिए पदनाम)। एनडी5 सबयूनिट के सी-टर्मिनस से एक असामान्य रूप से लंबे (110 Å) α-हेलिक्स (एचएल) से जुड़े दो ट्रांसमेम्ब्रेन हेलिकॉप्टरों से युक्त एक विस्तार का विस्तार होता है, जो कॉम्प्लेक्स के मैट्रिक्स-फेसिंग पक्ष के साथ गुजरते हुए, भौतिक रूप से तीनों को जोड़ता है एंटीपोर्ट-जैसी सबयूनिट, और संभवतः गठनात्मक पुनर्व्यवस्था के साथ युग्मित इलेक्ट्रॉन परिवहन में शामिल हैं। एक अन्य युग्मन तत्व, βH, ओवरलैपिंग और α-हेलिकॉप्टरों की एक श्रृंखला द्वारा बनता है और कॉम्प्लेक्स के विपरीत, पेरिप्लास्मिक पक्ष पर स्थित होता है। यह अभी भी पूरी तरह से अज्ञात है कि इलेक्ट्रॉन परिवहन प्रोटॉन स्थानांतरण के साथ कैसे जुड़ा हुआ है। ऐसा माना जाता है कि N2 क्लस्टर का शक्तिशाली नकारात्मक चार्ज आसपास के पॉलीपेप्टाइड्स को दूर धकेल सकता है, जिससे गठनात्मक परिवर्तन हो सकते हैं जो किसी तरह एक दूसरे से काफी दूर स्थित सभी एंटीपोर्ट-जैसे सबयूनिट में फैल जाते हैं। एक अन्य परिकल्पना से पता चलता है कि गठनात्मक परिवर्तन असामान्य रूप से लंबे यूबिकिनोन बाइंडिंग साइट को बेहद कम रेडॉक्स क्षमता और नकारात्मक चार्ज के साथ यूबिकिनोल क्यू−2 को स्थिर करने का कारण बनता है। गठनात्मक परिवर्तन और संबंधित प्रोटॉन परिवहन की गतिकी के कई विवरण अज्ञात हैं।
सबसे अधिक अध्ययन किया गया कॉम्प्लेक्स I अवरोधक रोटेनोन है (व्यापक रूप से जैविक कीटनाशक के रूप में उपयोग किया जाता है)। रोटेनोन और रोटेनोइड्स आइसोफ्लेवोनॉइड्स हैं जो कई उष्णकटिबंधीय पौधों की प्रजातियों की जड़ों में मौजूद होते हैं एंटोनिया (लोगानियासी), डेरिसऔर लोन्कोकार्पस (fabaceae). रोटेनोन का उपयोग लंबे समय से कीटनाशक और मछली के जहर के रूप में किया जाता रहा है, क्योंकि कीड़े और मछली के माइटोकॉन्ड्रिया इसके प्रति विशेष रूप से संवेदनशील होते हैं। यह ज्ञात है कि फ्रेंच गुयाना और अन्य दक्षिण अमेरिकी भारतीयों के स्वदेशी लोगों ने 17वीं शताब्दी की शुरुआत में मछली पकड़ने के लिए रोटेनोन युक्त पौधों का उपयोग किया था। रोटेनोन यूबिकिनोन बाइंडिंग साइट के साथ इंटरैक्ट करता है और मुख्य सब्सट्रेट के साथ प्रतिस्पर्धा करता है। यह दिखाया गया है कि रोटेनोन द्वारा कॉम्प्लेक्स I का दीर्घकालिक प्रणालीगत निषेध डोपामिनर्जिक न्यूरॉन्स (न्यूरोट्रांसमीटर डोपामाइन का स्राव) की चयनात्मक मृत्यु को प्रेरित कर सकता है। पियरिसिडिन ए, एक और शक्तिशाली कॉम्प्लेक्स I अवरोधक है जो संरचनात्मक रूप से यूबिकिनोन के समान है, समान तरीके से कार्य करता है। बार्बिट्यूरिक एसिड का व्युत्पन्न सोडियम अमाइटल भी इसी समूह से संबंधित है।
कॉम्प्लेक्स I के 50 से अधिक वर्षों के अध्ययन के बावजूद, उन अवरोधकों की खोज करना संभव नहीं हो पाया है जो कॉम्प्लेक्स के भीतर इलेक्ट्रॉन स्थानांतरण को रोकते हैं। हाइड्रोफोबिक अवरोधक जैसे रोटेनोन या पियरिसिडिन टर्मिनल एन2 क्लस्टर से यूबिकिनोन तक इलेक्ट्रॉन स्थानांतरण को बाधित करते हैं।
एक अन्य पदार्थ जो जटिल I को अवरुद्ध करता है वह NADH की ऑक्सीकरण प्रतिक्रिया में एडेनोसिन डाइफॉस्फेट राइबोस है। यह न्यूक्लियोटाइड बाइंडिंग साइट (एफएडी) पर एंजाइम से बंध जाता है।
कॉम्प्लेक्स I के कुछ सबसे शक्तिशाली अवरोधकों में एसिटोजेनिन परिवार शामिल है। इन पदार्थों को ND2 सबयूनिट के साथ रासायनिक क्रॉस-लिंक बनाते हुए दिखाया गया है, जो अप्रत्यक्ष रूप से यूबिकिनोन बाइंडिंग में ND2 की भूमिका को इंगित करता है। यह ध्यान रखना दिलचस्प है कि एसिटोजेनिन रोलिनीस्टैटिन -2 पहला जटिल I अवरोधक था जिसे रोटेनोन के अलावा किसी अन्य साइट पर बांधने के लिए खोजा गया था।
मधुमेहरोधी दवा मेटफॉर्मिन का मध्यम निरोधात्मक प्रभाव होता है; जाहिर है, दवा की यह संपत्ति इसकी क्रिया के तंत्र को रेखांकित करती है।
सक्सिनेट से इलेक्ट्रॉनों को पहले FAD में स्थानांतरित किया जाता है और फिर Fe-S क्लस्टर के माध्यम से Q में स्थानांतरित किया जाता है। कॉम्प्लेक्स में इलेक्ट्रॉन परिवहन एक प्रोटॉन ग्रेडिएंट की पीढ़ी के साथ नहीं होता है। सक्सिनेट के ऑक्सीकरण के दौरान गठित 2H+ झिल्ली के एक ही तरफ, यानी मैट्रिक्स में रहता है, और फिर क्विनोन की कमी के दौरान पुन: अवशोषित हो जाता है। इस प्रकार, कॉम्प्लेक्स II झिल्ली में प्रोटॉन ग्रेडिएंट के निर्माण में योगदान नहीं देता है और केवल सक्सिनेट से यूबिकिनोन तक एक इलेक्ट्रॉन ट्रांसपोर्टर के रूप में कार्य करता है।
सक्सेनेट के ऑक्सीकरण के परिणामस्वरूप, इसके इलेक्ट्रॉनों को एफएडी में स्थानांतरित किया जाता है और फिर क्लस्टर से क्लस्टर तक लौह-सल्फर समूहों की श्रृंखला के साथ स्थानांतरित किया जाता है। वहां, इन इलेक्ट्रॉनों को बंधन स्थल पर प्रतीक्षा कर रहे यूबिकिनोन अणु में स्थानांतरित कर दिया जाता है।
एक धारणा यह भी है कि एक इलेक्ट्रॉन को क्लस्टर से सीधे हीम तक पहुंचने से रोकने के लिए, एक विशेष गेट तंत्र संचालित होता है। गेट के लिए एक संभावित उम्मीदवार सबयूनिट बी का हिस्टिडाइन -207 है, जो सीधे लौह-सल्फर क्लस्टर और हीम के बीच स्थित है, बाध्य यूबिकिनोन के करीब है, और संभवतः इन रेडॉक्स केंद्रों के बीच इलेक्ट्रॉनों के प्रवाह को नियंत्रित कर सकता है।
जटिल II अवरोधकों के दो वर्ग हैं: कुछ सक्सिनेट बाइंडिंग पॉकेट को ब्लॉक करते हैं और अन्य यूबिकिनोल बाइंडिंग पॉकेट को ब्लॉक करते हैं। यूबिकिनोल की नकल करने वाले अवरोधकों में कार्बोक्सिन और थेनोयलट्राइफ्लुओरोएसीटोन शामिल हैं। सक्सिनेट के अवरोधक-एनालॉग में सिंथेटिक यौगिक मैलोनेट, साथ ही क्रेब्स चक्र, मैलेट और ऑक्सालोसेटेट के घटक शामिल हैं। दिलचस्प बात यह है कि ऑक्सालोएसीटेट सबसे शक्तिशाली कॉम्प्लेक्स II अवरोधकों में से एक है। ट्राइकार्बोक्सिलिक एसिड चक्र का एक सामान्य मेटाबोलाइट कॉम्प्लेक्स II को क्यों रोकता है यह स्पष्ट नहीं है, हालांकि यह सुझाव दिया गया है कि यह कॉम्प्लेक्स I में रिवर्स इलेक्ट्रॉन परिवहन को कम करके एक सुरक्षात्मक भूमिका निभा सकता है, जिसके परिणामस्वरूप सुपरऑक्साइड का निर्माण होता है।
यूबिकिनोल-मिमिकिंग अवरोधकों का उपयोग 1960 के दशक से कृषि में कवकनाशी के रूप में किया जाता रहा है। उदाहरण के लिए, कार्बोक्सिन का उपयोग मुख्य रूप से बेसिडिओमाइसीस के कारण होने वाली बीमारियों के लिए किया जाता है, जैसे स्टेम रस्ट और बेसिडिओमाइसीट रोग। राइज़ोक्टोनिया. हाल ही में, उन्हें दबे हुए रोगजनकों की एक विस्तृत श्रृंखला वाले अन्य यौगिकों द्वारा प्रतिस्थापित किया गया है। ऐसे यौगिकों में बोस्कालिड, पेन्थियोपाइराड और फ्लुओपाइरम शामिल हैं। कुछ कृषि संबंधी महत्वपूर्ण कवक इस नई पीढ़ी के अवरोधकों की कार्रवाई के प्रति संवेदनशील नहीं हैं।
साइटोक्रोम-बीसी1-कॉम्प्लेक्स (साइटोक्रोम कॉम्प्लेक्स ईसा पूर्व 1) या तो यूबिकिनोल-साइटोक्रोम सी-ऑक्सीडोरडक्टेज़, या कॉम्प्लेक्स III - इलेक्ट्रॉन परिवहन की श्वसन श्रृंखला का एक मल्टीप्रोटीन कॉम्प्लेक्स और माइटोकॉन्ड्रियल झिल्ली पर प्रोटॉन ग्रेडिएंट का सबसे महत्वपूर्ण जैव रासायनिक जनरेटर। यह मल्टीप्रोटीन ट्रांसमेम्ब्रेन कॉम्प्लेक्स माइटोकॉन्ड्रियल (साइटोक्रोम) द्वारा एन्कोड किया गया है बी) और परमाणु जीनोम।
साइटोक्रोम- bс 1-कॉम्प्लेक्स कम यूबिकिनोन को ऑक्सीकरण करता है और समीकरण के अनुसार साइटोक्रोम सी (ई°"=+0.25 वी) को कम करता है:
कॉम्प्लेक्स में इलेक्ट्रॉन परिवहन मैट्रिक्स (अंदर) से इंटरमेम्ब्रेन स्पेस (बाहर) में प्रोटॉन के स्थानांतरण और माइटोकॉन्ड्रियल झिल्ली पर एक प्रोटॉन ग्रेडिएंट की पीढ़ी से जुड़ा हुआ है। यूबिकिनोन से साइटोक्रोम सी तक परिवहन श्रृंखला के साथ गुजरने वाले प्रत्येक दो इलेक्ट्रॉनों के लिए, दो प्रोटॉन मैट्रिक्स से अवशोषित होते हैं, और चार और इंटरमेम्ब्रेन स्पेस में छोड़े जाते हैं। कम किया गया साइटोक्रोम सी जलीय अंश में झिल्ली के साथ चलता है और एक इलेक्ट्रॉन को अगले श्वसन परिसर, साइटोक्रोम ऑक्सीडेज में स्थानांतरित करता है।
होने वाली घटनाओं को क्यू-चक्र के रूप में जाना जाता है, जिसे 1976 में पीटर मिशेल द्वारा प्रतिपादित किया गया था। क्यू-चक्र का सिद्धांत यह है कि झिल्ली के पार एच+ का स्थानांतरण कॉम्प्लेक्स पर क्विनोन के ऑक्सीकरण और कमी के परिणामस्वरूप होता है। इस मामले में, क्विनोन क्रमशः झिल्ली के विभिन्न पक्षों से जलीय चरण से चुनिंदा रूप से 2H+ देते और लेते हैं।
कॉम्प्लेक्स III की संरचना में दो केंद्र या दो "पॉकेट" हैं, जिनमें क्विनोन बंध सकते हैं। उनमें से एक, क्यू आउट सेंटर, लौह-सल्फर क्लस्टर 2Fe-2S और हेम के बीच स्थित है बीएल झिल्ली के बाहरी हिस्से के पास, इंटरमेम्ब्रेन स्पेस का सामना कर रहा है। रिड्यूस्ड यूबिकिनोन (QH 2) इस पॉकेट में बंध जाता है। दूसरा, पॉकेट में क्यू, ऑक्सीकृत यूबिकिनोन (क्यू) को बांधने के लिए डिज़ाइन किया गया है और मैट्रिक्स के संपर्क में झिल्ली के अंदरूनी (अंदर) किनारे के पास स्थित है।
क्यू-चक्र के संचालन के लिए एक आवश्यक और विरोधाभासी स्थिति यह तथ्य है कि दो बंधन केंद्रों में सेमीक्विनोन का जीवनकाल और स्थिति अलग-अलग है। क्यू आउट सेंटर में, क्यू अस्थिर है और एक मजबूत कम करने वाले एजेंट के रूप में कार्य करता है जो कम क्षमता वाले हीम को ई दान करने में सक्षम है। एक अपेक्षाकृत लंबे समय तक जीवित रहने वाला Q - केंद्र में Q में बनता है, जिसकी क्षमता इसे ऑक्सीकरण एजेंट के रूप में कार्य करने की अनुमति देती है, जो हीम से इलेक्ट्रॉनों को स्वीकार करती है। बीएच। क्यू-चक्र का एक अन्य मुख्य बिंदु दो अलग-अलग पथों के साथ कॉम्प्लेक्स में शामिल दो इलेक्ट्रॉनों के विचलन से जुड़ा है। कॉम्प्लेक्स की क्रिस्टल संरचना के एक अध्ययन से पता चला है कि अन्य रेडॉक्स केंद्रों के सापेक्ष 2Fe-2S केंद्र की स्थिति बदल सकती है। यह पता चला कि रिस्के प्रोटीन में एक मोबाइल डोमेन है, जिस पर 2Fe-2S क्लस्टर वास्तव में स्थित है। एक इलेक्ट्रॉन को स्वीकार करने और कम होने पर, 2Fe-2S केंद्र अपनी स्थिति बदलता है, क्यू आउट सेंटर और हीम से दूर जाता है बी 60° के घूर्णन के साथ 17 तक एल और इस तरह साइटोक्रोम के करीब पहुंचता है सी. साइटोक्रोम को एक इलेक्ट्रॉन देने के बाद, 2Fe-2S केंद्र, इसके विपरीत, निकट संपर्क स्थापित करने के लिए Q आउट केंद्र के करीब चला जाता है। इस प्रकार, एक प्रकार का शटल कार्य करता है, यह गारंटी देता है कि दूसरा इलेक्ट्रॉन हेम्स तक जाता है बीभूमि बीएच। अब तक, यह एकमात्र उदाहरण है जहां कॉम्प्लेक्स में इलेक्ट्रॉन परिवहन प्रोटीन संरचना में एक मोबाइल डोमेन से जुड़ा हुआ है।
कॉम्प्लेक्स IV तक पहुंचने से पहले इलेक्ट्रॉनों का एक छोटा सा अंश परिवहन श्रृंखला छोड़ देता है। ऑक्सीजन में इलेक्ट्रॉनों के निरंतर रिसाव के परिणामस्वरूप सुपरऑक्साइड का निर्माण होता है। इस छोटी सी पार्श्व प्रतिक्रिया से प्रतिक्रियाशील ऑक्सीजन प्रजातियों के एक पूरे स्पेक्ट्रम का निर्माण होता है, जो बहुत विषैले होते हैं और विकृति विज्ञान और उम्र बढ़ने के विकास में महत्वपूर्ण भूमिका निभाते हैं)। इलेक्ट्रॉनिक लीक मुख्य रूप से क्यू इन साइट पर होते हैं। इस प्रक्रिया को एंटीमाइसिन ए द्वारा बढ़ावा दिया जाता है। यह हेम्स को ब्लॉक कर देता है बीउनकी कम अवस्था में, उन्हें सेमीक्विनोन क्यू पर इलेक्ट्रॉनों को छोड़ने से रोकता है, जिसके परिणामस्वरूप इसकी एकाग्रता में वृद्धि होती है। सेमीक्विनोन ऑक्सीजन के साथ प्रतिक्रिया करता है, जिससे सुपरऑक्साइड बनता है। परिणामस्वरूप सुपरऑक्साइड माइटोकॉन्ड्रियल मैट्रिक्स और इंटरमेम्ब्रेन स्पेस में प्रवेश करता है, जहां से यह साइटोसोल में प्रवेश कर सकता है। इस तथ्य को इस तथ्य से समझाया जा सकता है कि कॉम्प्लेक्स III संभवतः अनावेशित HOO के रूप में सुपरऑक्साइड का उत्पादन करता है, जो आवेशित सुपरऑक्साइड (O 2 -) की तुलना में बाहरी झिल्ली में अधिक आसानी से प्रवेश कर सकता है।
इनमें से कुछ पदार्थों का उपयोग कवकनाशी (जैसे स्ट्रोबिल्यूरिन डेरिवेटिव, जिनमें से सबसे प्रसिद्ध एज़ोक्सिस्ट्रोबिन, एक क्यू एक्सट साइट अवरोधक) और मलेरिया-रोधी (एटोवाक्वोन) के रूप में किया जाता है।
साइटोक्रोम सी ऑक्सीडेज (साइटोक्रोम ऑक्सीडेज) या साइटोक्रोम सी ऑक्सीजन ऑक्सीडोरडक्टेस, जिसे साइटोक्रोम एए 3 और कॉम्प्लेक्स IV के रूप में भी जाना जाता है, एरोबिक श्वसन इलेक्ट्रॉन परिवहन श्रृंखला का एक टर्मिनल ऑक्सीडेज है जो साइटोक्रोम से इलेक्ट्रॉनों के हस्तांतरण को उत्प्रेरित करता है। साथऑक्सीजन से पानी बनता है। साइटोक्रोम ऑक्सीडेज सभी यूकेरियोट्स के माइटोकॉन्ड्रिया की आंतरिक झिल्ली में मौजूद होता है, जहां इसे आमतौर पर कॉम्प्लेक्स IV कहा जाता है, साथ ही कई एरोबिक बैक्टीरिया की कोशिका झिल्ली में भी मौजूद होता है।
कॉम्प्लेक्स IV क्रमिक रूप से साइटोक्रोम सी के चार अणुओं को ऑक्सीकरण करता है और, चार इलेक्ट्रॉनों को स्वीकार करते हुए, ओ 2 को एच 2 ओ में कम कर देता है। ओ 2 की कमी के दौरान, चार एच + को कैप्चर किया जाता है
यूकेरियोट्स में - माइटोकॉन्ड्रिया की आंतरिक झिल्ली पर। वाहक उनकी रेडॉक्स क्षमता के अनुसार स्थित होते हैं; पूरी श्रृंखला के साथ इलेक्ट्रॉन परिवहन अनायास होता है।
प्रोटॉन क्षमता को एटीपी सिंथेज़ द्वारा एटीपी की रासायनिक बंधन ऊर्जा में परिवर्तित किया जाता है। ईटीसी और एटीपी सिंथेज़ के संयुग्म कार्य को ऑक्सीडेटिव फॉस्फोराइलेशन कहा जाता है।
माइटोकॉन्ड्रिया इलेक्ट्रॉन परिवहन श्रृंखला
- कॉम्प्लेक्स I (NADH डिहाइड्रोजनेज कॉम्प्लेक्स) NAD-H को ऑक्सीकृत करता है, इसमें से दो इलेक्ट्रॉन लेता है और उन्हें लिपिड-घुलनशील यूबिकिनोन में स्थानांतरित करता है, जो झिल्ली के अंदर कॉम्प्लेक्स III में फैल जाता है। उसी समय, कॉम्प्लेक्स I मैट्रिक्स से 2 प्रोटॉन और 2 इलेक्ट्रॉनों को माइटोकॉन्ड्रियन के इंटरमेम्ब्रेन स्पेस में पंप करता है।
- कॉम्प्लेक्स II (सक्सिनेट डिहाइड्रोजनेज) प्रोटॉन को पंप नहीं करता है, लेकिन सक्सिनेट के ऑक्सीकरण के कारण श्रृंखला में अतिरिक्त इलेक्ट्रॉन प्रदान करता है।
- कॉम्प्लेक्स III (साइटोक्रोम बीसी 1 कॉम्प्लेक्स) इलेक्ट्रॉनों को यूबिकिनोन से माइटोकॉन्ड्रियन की आंतरिक झिल्ली पर स्थित दो पानी में घुलनशील साइटोक्रोम सी में स्थानांतरित करता है। यूबिकिनोन 2 इलेक्ट्रॉनों को स्थानांतरित करता है, और साइटोक्रोम प्रति चक्र एक इलेक्ट्रॉन को स्थानांतरित करता है। उसी समय, यूबिकिनोन के 2 प्रोटॉन भी वहां से गुजरते हैं और कॉम्प्लेक्स के माध्यम से पंप किए जाते हैं।
- कॉम्प्लेक्स IV (साइटोक्रोम सी ऑक्सीडेज) 4 साइटोक्रोम अणुओं से 4 इलेक्ट्रॉनों के O2 में स्थानांतरण को उत्प्रेरित करता है और 4 प्रोटॉन को इंटरमेम्ब्रेन स्पेस में पंप करता है। कॉम्प्लेक्स में साइटोक्रोम ए और ए3 होते हैं, जिनमें हीम के अलावा, कॉपर आयन होते हैं।
ऑक्सीडेटिव क्षमता का प्रभाव
| संदर्भ पुस्तकें | आक्सीकारक | Ео´, В |
|---|---|---|
| एच 2 | 2 + | - 0,42 |
| एनएडी एच + एच+ | एनएडी+ | - 0,32 |
| एनएडीपी एच + एच+ | एनएडीपी+ | - 0,32 |
| फ्लेवोप्रोटीन (कम) | फ़्लेवोप्रोटीन (ऑक्सीकृत) | - 0,12 |
| कोएंजाइम Q H2 | कोएंजाइम Q | + 0,04 |
| साइटोक्रोम बी (Fe2+) | साइटोक्रोम बी (Fe3+) | + 0,07 |
| साइटोक्रोम सी 1 (Fe2+) | साइटोक्रोम सी 1 (Fe3+) | + 0,23 |
| साइटोक्रोमेस ए (Fe2+) | साइटोक्रोमेस A(Fe3+) | + 0,29 |
| साइटोक्रोमेस A3 (Fe2+) | साइटोक्रोमेस A3 (Fe3+) | +0,55 |
| H2O | ½ O2 | + 0,82 |
श्वसन श्रृंखला अवरोधक
कुछ पदार्थ कॉम्प्लेक्स I, II, III, IV के माध्यम से इलेक्ट्रॉन स्थानांतरण को रोकते हैं।
- कॉम्प्लेक्स I अवरोधक - बार्बिट्यूरेट्स, रोटेनोन, पियरिसिडिन
- कॉम्प्लेक्स II अवरोधक मैलोनेट है।
- कॉम्प्लेक्स III अवरोधक - एंटीमाइसिन ए, मायक्सोथियाज़ोल, स्टिग्मेटेलिन
- कॉम्प्लेक्स IV अवरोधक - हाइड्रोजन सल्फाइड, साइनाइड, कार्बन मोनोऑक्साइड, नाइट्रिक ऑक्साइड, सोडियम एजाइड
बैक्टीरिया की इलेक्ट्रॉन परिवहन श्रृंखला
माइटोकॉन्ड्रिया के विपरीत, बैक्टीरिया, इलेक्ट्रॉन दाताओं और स्वीकर्ता के एक बड़े समूह का उपयोग करते हैं, साथ ही उनके बीच विभिन्न इलेक्ट्रॉन स्थानांतरण मार्गों का भी उपयोग करते हैं। इन पथों को एक साथ चलाया जा सकता है, उदाहरण के लिए, ई कोलाईजब कार्बनिक पदार्थ के मुख्य स्रोत के रूप में ग्लूकोज युक्त माध्यम पर उगाया जाता है, तो यह दो एनएडीएच डिहाइड्रोजनेज और दो क्विनोलोक्सीडेस का उपयोग करता है, जिसका अर्थ है 4 इलेक्ट्रॉन परिवहन मार्गों की उपस्थिति। अधिकांश ईटीसी एंजाइम प्रेरक होते हैं और केवल तभी संश्लेषित होते हैं जब वे जिस मार्ग में प्रवेश करते हैं वह मांग में होता है।
कार्बनिक पदार्थों के अलावा, बैक्टीरिया में इलेक्ट्रॉन दाताओं में आणविक हाइड्रोजन, कार्बन मोनोऑक्साइड, अमोनियम, नाइट्राइट, सल्फर, सल्फाइड और डाइवैलेंट आयरन शामिल हो सकते हैं। एनएडीएच और सक्सिनेट डिहाइड्रोजनेज के बजाय, फॉर्मेट -, लैक्टेट -, ग्लिसराल्डिहाइड-3-फॉस्फेट डिहाइड्रोजनेज, हाइड्रोजनेज आदि मौजूद हो सकते हैं। एरोबिक परिस्थितियों में उपयोग किए जाने वाले ऑक्सीडेज के बजाय, ऑक्सीजन की अनुपस्थिति में, बैक्टीरिया रिडक्टेस का उपयोग कर सकते हैं जो विभिन्न को कम करते हैं अंतिम इलेक्ट्रॉन स्वीकर्ता: फ्यूमरेट रिडक्टेस, नाइट्रेट और नाइट्राइट रिडक्टेस, आदि।
यह सभी देखें
"इलेक्ट्रॉन परिवहन की श्वसन श्रृंखला" लेख के बारे में एक समीक्षा लिखें
टिप्पणियाँ
इलेक्ट्रॉन परिवहन की श्वसन श्रृंखला की विशेषता बताने वाला अंश
अंत में, चारों ओर सब कुछ हिलना शुरू हो गया, और यह पूरी भव्य पोशाक वाली भीड़, मानो जादू से, दो भागों में विभाजित हो गई, बिल्कुल बीच में एक बहुत चौड़ा, "बॉलरूम" मार्ग बन गया। और एक अत्यंत तेजस्वी महिला इस गलियारे से धीरे-धीरे आगे बढ़ रही थी... या यूं कहें कि एक जोड़ा आगे बढ़ रहा था, लेकिन उसके बगल वाला आदमी इतना सरल स्वभाव का और अगोचर था कि, अपने शानदार कपड़ों के बावजूद, उसकी पूरी शक्ल उसके बगल में फीकी पड़ गई उसका तेजस्वी साथी.खूबसूरत महिला वसंत की तरह लग रही थी - उसकी नीली पोशाक पूरी तरह से स्वर्ग के फैंसी पक्षियों और अद्भुत चांदी-गुलाबी फूलों के साथ कढ़ाई की गई थी, और असली ताजे फूलों की पूरी माला उसके रेशमी, जटिल स्टाइल वाले, राख के बालों पर एक नाजुक गुलाबी बादल में आराम कर रही थी। नाजुक मोतियों के कई धागे उसकी लंबी गर्दन के चारों ओर लिपटे हुए थे और उसकी अद्भुत त्वचा की असाधारण सफेदी से सचमुच चमक रहे थे। बड़ी-बड़ी चमचमाती नीली आँखें अपने आस-पास के लोगों का स्वागत करते हुए देख रही थीं। वह खुशी से मुस्कुराई और आश्चर्यजनक रूप से सुंदर थी....
फ्रांसीसी रानी मैरी एंटोनेट
वहीं, सबसे अलग खड़ा, एक्सल सचमुच बदल गया था!.. ऊबा हुआ युवक पलक झपकते ही कहीं गायब हो गया, और उसकी जगह... पृथ्वी पर सबसे सुंदर भावनाओं का जीवित अवतार खड़ा था, जो सचमुच धधकती निगाहों से उसे "भस्म" कर लिया। एक खूबसूरत महिला उसकी ओर आ रही थी...
"ओह-ओह... वह कितनी सुंदर है!.." स्टेला ने उत्साहपूर्वक साँस ली। - वह हमेशा बहुत खूबसूरत है!
- क्या, क्या तुमने उसे कई बार देखा है? - मैंने दिलचस्पी से पूछा।
- अरे हां! मैं अक्सर उसे देखने जाता हूं। वह वसंत की तरह है, है ना?
- और आप उसे जानते हैं?.. क्या आप जानते हैं वह कौन है?
"बेशक!.. वह बहुत दुखी रानी है," छोटी लड़की थोड़ा उदास हो गई।
- दुखी क्यों? ऐसा लगता है कि वह मुझसे बहुत खुश है,'' मुझे आश्चर्य हुआ।
"यह अभी है... और फिर वह मर जाएगी... वह बहुत डरावनी मरेगी - वे उसका सिर काट देंगे... लेकिन मुझे वह देखना पसंद नहीं है," स्टेला ने उदास होकर फुसफुसाया।
इस बीच, खूबसूरत महिला ने हमारे युवा एक्सल को पकड़ लिया और, उसे देखकर, एक पल के लिए आश्चर्य से ठिठक गई, और फिर, आकर्षक ढंग से शरमाते हुए, उसे बहुत प्यारी तरह से मुस्कुराया। किसी कारण से, मुझे ऐसा लगा कि दुनिया इन दो लोगों के आसपास एक पल के लिए थम गई... जैसे कि बहुत ही कम पल के लिए उन दोनों के अलावा उनके आसपास कुछ भी नहीं था और कोई भी नहीं था... लेकिन महिला चली गई पर, और वह जादुई क्षण हजारों छोटे-छोटे क्षणों में टूट गया, जो इन दो लोगों के बीच एक मजबूत चमकदार धागे में बंध गए, उन्हें कभी जाने नहीं दिया...
एक्सल पूरी तरह से स्तब्ध खड़ा था और, फिर से आसपास किसी को भी न देखकर, अपनी खूबसूरत महिला की देखभाल की, और उसका जीता हुआ दिल धीरे-धीरे उसके साथ चला गया... उसने गुजरती हुई युवा सुंदरियों की ओर उसकी ओर देखते हुए ध्यान नहीं दिया, और उनकी बातों का कोई जवाब नहीं दिया। चमकता हुआ, मुस्कुराहट को आमंत्रित करता हुआ।
काउंट एक्सल फ़र्सन मैरी एंटोनेट
एक व्यक्ति के रूप में, एक्सल, जैसा कि वे कहते हैं, "अंदर और बाहर दोनों" बहुत आकर्षक था। वह लंबा और सुंदर था, बड़ी गंभीर भूरी आँखों वाला, हमेशा मिलनसार, आरक्षित और विनम्र था, जो महिलाओं और पुरुषों दोनों को समान रूप से आकर्षित करता था। उनका सही, गंभीर चेहरा शायद ही कभी मुस्कुराहट से चमकता था, लेकिन अगर ऐसा हुआ, तो ऐसे क्षण में एक्सल बस अप्रतिरोध्य हो गया... इसलिए, आकर्षक महिला आधे के लिए उसकी ओर ध्यान बढ़ाना पूरी तरह से स्वाभाविक था, लेकिन, उनका सामान्य अफसोस, एक्सल को केवल इस बात में रुचि थी कि पूरी दुनिया में केवल एक ही प्राणी है - उसकी अनूठी, सुंदर रानी...
- क्या वे एक साथ रहेंगे? - मैं इसे बर्दाश्त नहीं कर सका। - वे दोनों बहुत सुंदर हैं!
स्टेला बस उदास होकर मुस्कुराई और तुरंत हमें इस असामान्य और किसी तरह बहुत ही मार्मिक कहानी के अगले "एपिसोड" में ले गई...
हमने खुद को एक बहुत ही आरामदायक, फूलों की सुगंध वाले, छोटे ग्रीष्मकालीन बगीचे में पाया। चारों ओर, जहाँ तक नज़र जा सकती थी, एक शानदार हरा-भरा पार्क था, जो कई मूर्तियों से सजा हुआ था, और दूरी पर एक छोटे शहर की तरह दिखने वाला एक आश्चर्यजनक विशाल पत्थर का महल देखा जा सकता था। और इस सब "भव्य", थोड़ा दमनकारी, आसपास की भव्यता के बीच, केवल यह उद्यान, जो पूरी तरह से चुभती नज़रों से सुरक्षित है, ने वास्तविक आराम और कुछ प्रकार की गर्म, "घरेलू" सुंदरता की भावना पैदा की ...
गर्मी की शाम की गर्मी से तेज, खिले हुए बबूल, गुलाब और कुछ और चीज़ों की चक्करदार मीठी गंध हवा में थी जिसे मैं पहचान नहीं सका। छोटे तालाब की साफ सतह के ऊपर, जैसे कि एक दर्पण में, नरम गुलाबी पानी की लिली के विशाल कप और सोने के लिए तैयार आलसी, शाही हंसों के बर्फ-सफेद "फर कोट" प्रतिबिंबित हो रहे थे। एक खूबसूरत युवा जोड़ा एक तालाब के चारों ओर एक छोटे, संकरे रास्ते पर चल रहा था। दूर कहीं, संगीत सुनाई दे रहा था, हँसमुख महिला हँसी घंटियों की तरह झिलमिला रही थी, कई लोगों की हर्षित आवाज़ें सुनाई दे रही थीं, और केवल इन दोनों के लिए दुनिया यहीं रुक गई, पृथ्वी के इस छोटे से कोने में, जहाँ उस पल कोमल आवाज़ें थीं पक्षियों की ध्वनि केवल उन्हीं के लिए थी; केवल उनके लिए एक चंचल, हल्की हवा गुलाब की पंखुड़ियों में सरसराहट करती है; और केवल उनके लिए, एक पल के लिए, समय मददगार बनकर रुक गया, जिससे उन्हें अकेले रहने का मौका मिला - सिर्फ एक पुरुष और एक महिला जो अलविदा कहने के लिए यहां आए थे, यह भी नहीं जानते थे कि यह हमेशा के लिए रहेगा या नहीं...
वह महिला छोटे हरे फूलों से सजी अपनी मामूली, सफेद ग्रीष्मकालीन पोशाक में आकर्षक और किसी तरह "हवादार" थी। उसके अद्भुत राख जैसे बाल हरे रिबन से बंधे हुए थे, जिससे वह एक प्यारी वन परी की तरह लग रही थी। वह इतनी युवा, शुद्ध और विनम्र लग रही थी कि मैं तुरंत उसमें उस रानी की राजसी और शानदार सुंदरता को नहीं पहचान सका, जिसे मैंने कुछ ही मिनट पहले उसकी शानदार "औपचारिक" सुंदरता में देखा था।
संरचनात्मक और कार्यात्मक रूप से संबंधित ट्रांसमेम्ब्रेन प्रोटीन और इलेक्ट्रॉन वाहक की एक प्रणाली। यह आपको आणविक ऑक्सीजन द्वारा NAD*H और FADH2 के ऑक्सीकरण के दौरान जारी ऊर्जा को श्रृंखला के साथ एक इलेक्ट्रॉन के अनुक्रमिक हस्तांतरण के कारण एक ट्रांसमेम्ब्रेन प्रोटॉन क्षमता के रूप में संग्रहीत करने की अनुमति देता है, जो झिल्ली के माध्यम से प्रोटॉन के पंपिंग के साथ जुड़ा होता है। यूकेरियोट्स में परिवहन श्रृंखला आंतरिक माइटोकॉन्ड्रियल झिल्ली पर स्थानीयकृत होती है। श्वसन श्रृंखला में 4 मल्टीएंजाइम कॉम्प्लेक्स होते हैं। एक अन्य कॉम्प्लेक्स भी है जो इलेक्ट्रॉन स्थानांतरण में शामिल नहीं है, लेकिन एटीपी को संश्लेषित करता है।
पहला - सीओए ऑक्सीडोरडक्टेस।
1.एनएडीएच से इलेक्ट्रॉनों को स्वीकार करता है और उन्हें कोएंजाइम क्यू (यूबिकिनोन) में स्थानांतरित करता है। 2. 4 H+ आयनों को आंतरिक माइटोकॉन्ड्रियल झिल्ली की बाहरी सतह पर स्थानांतरित करता है।
दूसरा-एफएडी-निर्भर डिहाइड्रोजनेज।
1. साइटोक्रोम सी ऑक्सीडोरडक्टेस द्वारा एफएडी में कमी।
2.कोएंजाइम Q से इलेक्ट्रॉन प्राप्त करता है और उन्हें साइटोक्रोम c में स्थानांतरित करता है।
3.2 H+ आयनों को आंतरिक माइटोकॉन्ड्रियल झिल्ली की बाहरी सतह पर स्थानांतरित करता है।
चौथा-साइटोक्रोम सी-ऑक्सीजन ऑक्सीडोरडक्टेस।
1. साइटोक्रोम सी से इलेक्ट्रॉनों को स्वीकार करता है और पानी बनाने के लिए उन्हें ऑक्सीजन में स्थानांतरित करता है।
2. 4 H+ आयनों को आंतरिक माइटोकॉन्ड्रियल झिल्ली की बाहरी सतह पर स्थानांतरित करता है। एरोबिक स्थितियों के तहत डिहाइड्रोजनेज द्वारा सब्सट्रेट्स से अलग किए गए सभी हाइड्रोजन परमाणु एनएडीएच या एफएडीएच 2 के हिस्से के रूप में आंतरिक माइटोकॉन्ड्रियल झिल्ली तक पहुंचते हैं।
जैसे ही इलेक्ट्रॉन चलते हैं, वे ऊर्जा खो देते हैं -> ऊर्जा एच प्रोटॉन को पंप करने पर कॉम्प्लेक्स द्वारा खर्च की जाती है। एच आयनों का स्थानांतरण कड़ाई से परिभाषित क्षेत्रों -> संयुग्मन क्षेत्रों में होता है। परिणाम: एटीपी का उत्पादन होता है: एच+ आयन एटीपी सिंथेज़ से गुजरते हुए अपनी ऊर्जा खो देते हैं। इस ऊर्जा का एक भाग एटीपी संश्लेषण पर खर्च होता है। दूसरा भाग ऊष्मा के रूप में नष्ट हो जाता है।
माइटोकॉन्ड्रियल श्वसन श्रृंखला में 5 मल्टीएंजाइम कॉम्प्लेक्स होते हैं, जिनकी उपइकाइयाँ परमाणु और माइटोकॉन्ड्रियल जीन दोनों द्वारा एन्कोड की जाती हैं। कोएंजाइम Q10 और साइटोक्रोम c इलेक्ट्रॉन परिवहन में शामिल होते हैं। इलेक्ट्रॉन NAD*H और FAD"H अणुओं से आते हैं और श्वसन श्रृंखला के साथ ले जाए जाते हैं। जारी ऊर्जा का उपयोग प्रोटॉन को माइटोकॉन्ड्रिया की बाहरी झिल्ली तक ले जाने के लिए किया जाता है, और परिणामी इलेक्ट्रोकेमिकल ग्रेडिएंट का उपयोग जटिल V का उपयोग करके एटीपी को संश्लेषित करने के लिए किया जाता है। माइटोकॉन्ड्रियल श्वसन श्रृंखला
44. श्वसन श्रृंखला में इलेक्ट्रॉन वाहकों का अनुक्रम और संरचना
1 जटिल. NADH-CoQ ऑक्सीडोरडक्टेस
इस कॉम्प्लेक्स का कामकाजी नाम NADH डिहाइड्रोजनेज भी है, इसमें FMN (फ्लेविन मोनोन्यूक्लियोटाइड), 22 प्रोटीन अणु होते हैं, जिनमें से 5 आयरन-सल्फर प्रोटीन होते हैं जिनका कुल आणविक भार 900 kDa तक होता है।
NADH से इलेक्ट्रॉनों को स्वीकार करता है और उन्हें कोएंजाइम Q (यूबिकिनोन) में स्थानांतरित करता है।
4 H+ आयनों को आंतरिक माइटोकॉन्ड्रियल झिल्ली की बाहरी सतह पर स्थानांतरित करता है।
2 जटिल. एफएडी-निर्भर डिहाइड्रोजनेज
इसमें आंतरिक झिल्ली पर स्थित FAD-निर्भर एंजाइम शामिल हैं - उदाहरण के लिए, एसाइल-एससीओए डिहाइड्रोजनेज (फैटी एसिड ऑक्सीकरण), सक्सिनेट डिहाइड्रोजनेज (ट्राइकारबॉक्सिलिक एसिड चक्र), माइटोकॉन्ड्रियल ग्लिसरॉल-3-फॉस्फेट डिहाइड्रोजनेज (माइटोकॉन्ड्रिया में एनएडीएच शटल)।
रेडॉक्स प्रतिक्रियाओं में एफएडी की कमी।
आंतरिक माइटोकॉन्ड्रियल झिल्ली के लौह-सल्फर प्रोटीन में FADN2 से इलेक्ट्रॉनों का स्थानांतरण सुनिश्चित करना। ये इलेक्ट्रॉन फिर कोएंजाइम Q में चले जाते हैं।
46. ऑक्सीकरण और फास्फारिलीकरण के पृथक्करण के जैव रासायनिक तंत्र, उन्हें उत्पन्न करने वाले कारकश्वसन और फास्फारिलीकरण का पृथक्करण
कुछ रसायन (प्रोटोनोफोर्स) एटीपी सिंथेज़ के प्रोटॉन चैनलों को दरकिनार करते हुए, झिल्ली के माध्यम से मैट्रिक्स में झिल्ली के माध्यम से प्रोटॉन या अन्य आयनों (आयनोफोर्स) को ले जा सकते हैं। परिणामस्वरूप, इलेक्ट्रोकेमिकल क्षमता गायब हो जाती है और एटीपी संश्लेषण बंद हो जाता है। इस घटना को श्वसन और फास्फारिलीकरण का अनयुग्मन कहा जाता है। अनयुग्मन के परिणामस्वरूप एटीपी की मात्रा कम हो जाती है और एडीपी बढ़ जाती है। इस मामले में, NADH और FADH2 के ऑक्सीकरण की दर बढ़ जाती है, और अवशोषित ऑक्सीजन की मात्रा भी बढ़ जाती है, लेकिन ऊर्जा गर्मी के रूप में निकलती है, और P/O अनुपात तेजी से कम हो जाता है। एक नियम के रूप में, अनकप्लर्स लिपोफिलिक पदार्थ होते हैं जो झिल्ली की लिपिड परत से आसानी से गुजरते हैं। इन पदार्थों में से एक 2,4-डाइनिट्रोफेनोल (चित्र 6-17) है, जो आसानी से आयनित रूप से गैर-आयनित रूप में गुजरता है, इंटरमेम्ब्रेन स्पेस में एक प्रोटॉन को जोड़ता है और इसे मैट्रिक्स में स्थानांतरित करता है।
अनकप्लर्स के उदाहरण कुछ दवाएं भी हो सकते हैं, उदाहरण के लिए, डाइकुमरोल - एक थक्कारोधी (धारा 14 देखें) या शरीर में बनने वाले मेटाबोलाइट्स, बिलीरुबिन - अपचय का एक उत्पाद (धारा 13 देखें), थायरोक्सिन - एक थायराइड हार्मोन (अनुभाग देखें) 11)। ये सभी पदार्थ केवल उच्च सांद्रता पर ही अनयुग्मन प्रभाव प्रदर्शित करते हैं।
एडीपी या अकार्बनिक फॉस्फेट की कमी होने पर फॉस्फोराइलेशन को बंद करने से श्वसन में रुकावट (श्वसन नियंत्रण प्रभाव) होती है। माइटोकॉन्ड्रियल झिल्ली को नुकसान पहुंचाने वाले बड़ी संख्या में प्रभाव ऑक्सीकरण और फॉस्फोराइलेशन के बीच युग्मन को बाधित करते हैं, जिससे एटीपी संश्लेषण (अनकपलिंग प्रभाव) की अनुपस्थिति में भी इलेक्ट्रॉन स्थानांतरण हो सकता है।
1. कुल आउटपुट:
1 एटीपी अणु को संश्लेषित करने के लिए 3 प्रोटॉन की आवश्यकता होती है।
2. ऑक्सीडेटिव फास्फारिलीकरण के अवरोधक:
अवरोधक वी कॉम्प्लेक्स को रोकते हैं:
ओलिगोमाइसिन - एटीपी सिंथेज़ के प्रोटॉन चैनलों को ब्लॉक करता है।
एट्रैक्टाइलोसाइड, साइक्लोफाइलिन - ट्रांसलोकेस को ब्लॉक करें।
3. ऑक्सीडेटिव फास्फारिलीकरण के अनयुग्मक:
अनकप्लर्स लिपोफिलिक पदार्थ होते हैं जो प्रोटॉन को स्वीकार करने और वी कॉम्प्लेक्स (इसके प्रोटॉन चैनल) को दरकिनार करते हुए माइटोकॉन्ड्रिया की आंतरिक झिल्ली के माध्यम से स्थानांतरित करने में सक्षम होते हैं। डिस्कनेक्टर्स:
प्राकृतिक - लिपिड पेरोक्सीडेशन, लंबी श्रृंखला फैटी एसिड के उत्पाद; थायराइड हार्मोन की बड़ी खुराक.
कृत्रिम - डाइनिट्रोफेनॉल, ईथर, विटामिन के डेरिवेटिव, एनेस्थेटिक्स।