Молекулы состоящие из атомов разного вида. Строение вещества - молекулы
Квант (от нем. Quant -«квант», от лат. quantum - «сколько») - неделимая порция какой-либо элементарной частицы или величины вфизике (например, количество (порция) электромагнитного излучения, которое в единичном акте способен излучить или поглотить или др. квантовая система; элементарная частица, то же, что фотон). В основе понятия лежит представление квантовой механики о том, что некоторые физические величины могут принимать только определённые значения (говорят, что физическая величина квантуется ).
В некоторых важных частных случаях эта величина или шаг её изменения могут быть только целыми кратными некоторого фундаментального значения - и последнее называют квантом . Например, энергия монохроматического электромагнитного излученияугловой частоты ω может принимать значения (N+1/2)ℏω, где ℏ - редуцированная постоянная Планка, а N - целое число. В этом случае ℏω имеет смысл энергии кванта излучения (иными словами, фотона), а N - смысл числа́ этих квантов (фотонов). Именно в этом смысле термин квант был впервые введен Максом Планком в его классической работе 1900 года - первой работе по квантовой теории, заложившей ее основу.
Вокруг идеи квантования с начала 1900-х годов развилась полностью новая физическая концепция, обычно называемая квантовой физикой (например, количество (порция) электромагнитного излучения, которое в единичном акте способен излучить или поглотить или др. квантовая система; элементарная частица, то же, что фотон).
Ныне прилагательное «квантовый» используется в названии ряда областей физики (квантовая механика, квантовая теория поля,квантовая оптика и т. д.). Широко применяется термин квантование, означающий построение квантовой теории некоторой системы или переход от её классического описания к квантовому. Тот же термин употребляется для обозначения ситуации, в которой физическая величина может принимать только дискретные значения - например, говорят, что энергия электрона в атоме «квантуется». Сам же термин «квант» в настоящее время имеет в физике довольно ограниченное применение. Иногда его употребляют для обозначения частиц или квазичастиц, соотвествующих бозонным полям взаимодействия (фотон - квант электромагнитного поля, фонон - квант поля звуковых волн в кристалле, гравитон - гипотетический квант гравитационного поля и т. д.), также о таких частицах говорят как о «квантах возбуждения» или просто «возбуждениях» соответствующих полей.
Кроме того, по традиции «квантом действия» иногда называют постоянную Планка. В современном понимании это название может иметь тот смысл, что постоянная Планка является естественной квантовой единицей измерения действия и других физических величин такой же размерности (например, момента импульса).
Кварк - фундаментальная частица в Стандартной модели, обладающая электрическим зарядом, кратным e /3, и не наблюдающаяся в свободном состоянии, но входящая в составадронов (сильновзаимодействующих частиц, таких как протоны и нейтроны). Кварки являются бесструктурными, точечными частицами; это проверено вплоть до масштаба примерно 5·10 −18 м, что примерно в 20 тысяч раз меньше размера протона.
В настоящее время известно 6 разных «сортов» (чаще говорят - «ароматов») кварков, свойства которых даны в таблице. Кроме того, для калибровочного описания сильного взаимодействия постулируется, что кварки обладают и дополнительной внутренней характеристикой, называемой «цвет». Каждому кварку соответствует антикварк с противоположными квантовыми числами.
Гипотеза о том, что адроны построены из специфических субъединиц, была впервые выдвинута М. Гелл-Манном и, независимо от него, Дж. Цвейгом в 1964 году.
Нукло́ны (от лат. nucleus - ядро) - частицы, из которых построены атомные ядра. Нуклоны представлены протонами и нейтронами.
С точки зрения электромагнитного взаимодействия протон и нейтрон разные частицы, так как протон электрически заряжен, а нейтрон - нет. Однако с точки зрения сильного взаимодействия, которое является определяющим в масштабе атомных ядер, эти частицы неразличимы, поэтому и был введен термин «нуклон», а протон и нейтрон стали рассматриваться как два различных состояния нуклона, различающихся проекцией изотопического спина. Близость свойств изоспиновых состояний нуклона является одним из проявлений изотопической инвариантности.
Атом - это наименьшая частица химического элемента, сохраняющая все его химические свойства. Атом состоит из ядра, имеющего положительный электрический заряд, и отрицательно заряженных электронов. Заряд ядра любого химического элемента равен произведению Z на e, где Z - порядковый номер данного элемента в периодической системе химических элементов, е - величина элементарного электрического заряда.
Электрон
- мельчайшая частица вещества с отрицательным электрическим зарядом е=1,6·10 -19 кулона, принятым за элементарный электрический заряд. Электроны, вращаясь вокруг ядра, располагаются на электронных оболочках К, L, М и т. д. К - оболочка, ближайшая к ядру. Размер атома определяется размером его электронной оболочки. Атом может терять электроны и становиться положительным ионом или присоединять электроны и становиться отрицательным ионом. Заряд иона определяет число потерянных или присоединенных электронов. Процесс превращения нейтрального атома в заряженный ион называется ионизацией.
Атомное ядро
(центральная часть атома) состоит из элементарных ядерных частиц - протонов и нейтронов. Радиус ядра примерно в сто тысяч раз меньше радиуса атома. Плотность атомного ядра чрезвычайно велика. Протоны
- стабильные элементарные частицы, имеющие единичный положительный электрический заряд и массу, в 1836 раз большую, чем масса электрона. Протон представляет собой ядро атома самого легкого элемента - водорода. Число протонов в ядре равно Z. Нейтрон
- нейтральная (не имеющая электрического заряда) элементарная частица с массой, очень близкой к массе протона. Поскольку масса ядра складывается из массы протонов и нейтронов, то число нейтронов в ядре атома равно А - Z, где А - массовое число данного изотопа (см. Периодическая система химических элементов). Протон и нейтрон, входящие в состав ядра, называются нуклонами. В ядре нуклоны связаны особыми ядерными силами.
В атомном ядре имеется огромный запас энергии, которая высвобождается при ядерных реакциях. Ядерные реакции возникают при взаимодействии атомных ядер с элементарными частицами или с ядрами других элементов. В результате ядерных реакций образуются новые ядра. Например, нейтрон может переходить в протон. В этом случае из ядра выбрасывается бета-частица, т. е. электрон.
Переход в ядре протона в нейтрон может осуществляться двумя путями: либо из ядра испускается частица с массой, равной массе электрона, но с положительным зарядом, называемая позитроном (позитронный распад), либо ядро захватывает один из электронов с ближайшей к нему К-оболочки (К-захват).
Иногда образовавшееся ядро обладает избытком энергии (находится в возбужденном состоянии) и, переходя в нормальное состояние, выделяет лишнюю энергию в виде электромагнитного излучения с очень малой длиной волны - гамма-излучение. Энергия, выделяющаяся при ядерных реакциях, практически используется в различных отраслях промышленности.
Молекула (франц. molecule, от лат. moles - масса) - наименьшая способная к самостоятельному существованию частица вещества, обладающая его химическими свойствами.
Учение о строении и свойствах молекул приобрело исключительный интерес для познания субмикроскопической структуры клеток и тканей, а также механизма биологических процессов на молекулярном уровне. Большие успехи в изучении структуры М. и, в частности, М. таких биополимеров, как белки и нуклеиновые кислоты, показали, что важнейшие функции этих веществ в организмах осуществляются на уровне отдельных молекул и поэтому должны исследоваться как молекулярные явления. Установлено, например, что такие функции белков, как ферментативная, структурная, сократительная, иммунная, транспортная (обратимое связывание и перенос жизненно необходимых веществ) разыгрываются на молекулярном уровне и непосредственно определяются структурой и свойствами М. этих веществ. Наследственность и изменчивость организмов связаны с особой структурой и свойствами М. нуклеиновых кислот, в которых зафиксирована вся генетическая информация, необходимая для синтеза белков организма. Небольшие отклонения в структуре или составе молекул ряда биологически важных веществ или изменения в молекулярном механизме некоторых обменных процессов являются причиной возникновения ряда заболеваний (например, серповидноклеточная анемия, наследственная галактоземия, сахарный диабет и др.), называемых молекулярными болезнями.
Молекула каждого вещества состоит из определенного числа атомов (см.) одного химического элемента (простое вещество) или различных элементов (сложное вещество), объединенных посредством химических (валентных) связей. Состав М. выражают химической формулой, в которой знаки элементов указывают вид атомов, образующих М., а числа, стоящие справа внизу, показывают, сколько атомов каждого элемента входит в состав М. Так, из химической формулы глюкозы СвН12Ое следует, что М. глюкозы состоит из 6 атомов углерода, 12 атомов водорода и 6 атомов кислорода. Молекулы инертных газов и паров некоторых металлов одноатомны. Это самые простые М. Наиболее сложными являются М. белков (см.), нуклеиновых кислот (см.) и других биополимеров, состоящие из многих тысяч атомов.
Все вещества состоят из крошечных частиц - атомов. Атомы соединяются в молекулы, крупнейшие из которых имеют сложное строение, состоящее из тысяч атомов.
О том, что все сущее состоит из частиц, знали еще древние греки. Около 420 г. до н. э. философ Демокрит поддержал гипотезу, что материя состоит из крошечных, неделимых частиц. По-гречески atomos означает "неделимый", поэтому эти частицы назвали атомами.
Другие философы придерживались иной точки зрения, и в IV веке до н. э. Аристотель высказался в поддержку мнения, согласно которому материя состоит из различных сочетаний так называемых четырех стихий - земли, воздуха, огня и воды. Эта идея получила широкое распространение и легла в основу алхимии - примитивной формы химии, господствовавшей в науке до XVII века.
Одной из главных задач алхимии было создание "эликсира жизни" - снадобья, которое позволило бы человеку жить вечно. Другая заключалась в создании богатств путем превращения обычных металлов в золото. Многие алхимики утверждали, что решили эти задачи, однако никто из них так и не добился реального успеха.
Переворот в науке
Некоторые ученые продолжали придерживаться мнения, что материя состоит из атомов, но только в начале XIX века были получены экспериментальные данные, подтверждающие эту теорию. Английский химик и писатель Джон Дальтон проводил опыты с газами и изучал пути их соединения. Так, он обнаружил, что кислород и водород, образуя воду, всегда соединяются в одних и тех же пропорциях по массе. Другие ученые также сталкивались с подобными данными, но именно Дальтон впервые осознал их значение. Он сделал вывод, что вещества состоят из атомов, и что все атомы простого вещества имеют одинаковую массу. При соединении простых веществ количества соединяющихся атомов находятся в определенной неизменной пропорции. Атомистика Дальтона объясняла, почему вещества соединяются в неизменной массовой пропорции, а также явилась основой для детального изучения материи. Вещества состоят из атомов, а из чего состоят атомы? Первые ключи к разгадке этой тайны появились в конце XIX века, когда исследователи изучали прохождение электричества через разрядные трубки, содержащие разреженный воздух. Иногда стенки трубки излучали зеленый свет при подаче высокого напряжения на две металлические пластины - электроды. Свечение возникало при попадании невидимых лучей от отрицательного электрода, или катода, на стенки трубки.
В 1890-х годах английский физик Дж. Томсон доказал, что эти катодные лучи (как их тогда называли) - не что иное, как потоки отрицательно заряженных частиц. Предполагалось, что эти частицы исходят из атомов, хотя их расположение внутри атомов оставалось неясным. Томсон высказал предположение, что атом может быть похож на рождественский пудинг, в котором большая, но легкая по массе положительно заряженная сфера усеяна многочисленными отрицательно заряженными частицами (электронами). Однако различные опыты по изучению строения атома доказали, что это - безусловно ошибочная теория.
Строение атома
В 1911 году Эрнест Резерфорд, британский физик, уроженец Новой Зеландии, работавший вместе с Томсоном, предложил строение атома, реально объясняющее его поведение во время экспериментов. Резерфорд предположил, что центр (или ядро) атома имеет положительный заряд и относительно большую массу, а вокруг ядра вращаются крайне легкие и отрицательно заряженные электроны.
Однако Резерфорд не осознавал, что обычно в ядре атома находятся как положительно заряженные, так и нейтральные частицы. Существование положительно заряженных частиц было признано в 1920 г., и они получили название протоны. В 1932 г. английский физик Джеймс Чэдвик открыл незаряженные частицы и назвал их нейтронами. В результате картина строения атома была завершена и с тех пор является основой нашего понимания материи.
Элементы
Любое вещество, в котором все атомы имеют одинаковое количество протонов, называется элементом. Число протонов в каждом атоме - атомный номер элемента. Существуют 92 природных элемента, их атомы имеют от 1 до 92 протонов. Кроме того, некоторые другие элементы с еще большим числом протонов в атоме можно получить с помощью устройства под названием ускоритель элементарных частиц. К природным элементам относятся железо, ртуть и водород.
Во многих веществах атомы объединяются в группы, называемые молекулами. Так, газ водород состоит из молекул, каждая из которых содержит два атома водорода. Часто, однако, молекулы вещества состоят из атомов более одного элемента. Такие вещества называются соединениями. Например, вода является соединением, где каждая молекула состоит из двух атомов водорода и одного атома кислорода. Во многих молекулах насчитывается гораздо большее количество атомов. Некоторые белковые молекулы представляют собой сложные соединения из нескольких тысяч атомов. Некоторые природные элементы встречаются только в соединениях. Так, натрий - это металл, настолько легко соединяющийся с другими веществами, что его нельзя обнаружить в чистом виде. Он широко известен в сочетании с хлором в виде хлорида натрия - поваренной соли.
Атомы в молекулах связываются различными путями, при этом они разделяют между собой электроны или обмениваются ими. Двумя простыми видами химической связи являются ковалентная и ионная.
Ковалентная связь возникает, когда атомы имеют общие электроны. Так, молекула водородного газа состоит из двух атомов водорода, связанных ковалентной связью. Единственный электрон каждого атома водорода вращается вокруг ядер обоих атомов, связывая их воедино.
В случае ионной связи один атом передает электроны другому атому. В результате возникает электрическая сила, связывающая атомы воедино. Как правило, количество положительно заряженных протонов и отрицательно заряженных электронов в атоме одинаково. Их положительные и отрицательные заряды уравновешивают друг друга, и поэтому атом не имеет общего заряда. Однако в атоме, отдающем электроны, создается избыток положительного заряда, а атом, получающий электроны, приобретает общий отрицательный заряд. Такие заряженные атомы называются ионами. Ионы противоположных зарядов притягиваются друг к другу, и именно это электрическое притяжение удерживает атомы вместе при ионной связи. Например, молекула поваренной соли формируется с помощью ионной связи, когда атом натрия передает электрон атому хлора.
Все атомы одного вещества имеют одинаковое количество протонов, но различное количество нейтронов. Так, в углероде ядро большинства атомов содержит шесть нейтронов, но примерно в каждом сотом из них имеется семь нейтронов. Эти различные типы атомов одного и того же элемента называются изотопами. Все изотопы данного элемента обладают одинаковыми химическими свойствами - все они соединяются с другими веществами и образуют одни и те же химические соединения. Но отдельные физические свойства изотопов различаются - например, они имеют разные точки замерзания или кипения.
Говоря о конкретном изотопе того или иного элемента, ученые называют его массовое число. Например, углерод-12 - это обычный природный изотоп углерода. Его атом содержит шесть протонов и шесть нейтронов. Более редкий природный изотоп, в ядре каждого атома которого находится лишний нейтрон, называется углерод-13.
Атомный вес
Протон и нейтрон имеют почти одинаковую массу, которая более чем в 1800 раз превышает массу электрона. Поэтому когда речь идет о массе атома, как правило, не будет ошибкой ссылаться на его массовое число.
Атомный вес элемента, или его относительная атомная масса, обычно представляет собой среднюю массу смеси изотопов, встречающихся в природе. Молекулярный вес вещества, или его относительная молекулярная масса, - это сумма атомных весов всех атомов в одной молекуле данного вещества.
Многосложный атом
С тех пор экспериментировавшие с ускорителями ученые открыли сотни других видов частиц в атомах. Но, к счастью, простая модель атома достаточна для того, чтобы объяснить большую часть свойств материи.
Строение вещества - одна из самых распространенных тем для спор древних философов. С древнейших времен люди строили предположения по поводу того, как устроена окружающая нас материя, из чего сделаны все предметы. Были очень распространены точки зрения, будто материя состоит из огня, воды, воздуха или же земли - 4 элемента.
Теория Демокрита о строении вещества
Среди прочих была и точка зрения древнегреческого ученого Демокрита о том, что материя состоит из мельчайших неделимых частиц. Частицы эти называли атомами, поскольку атом с древнегреческого переводится как "неделимый". Это предположение Демокрита долгое время не привлекало к себе внимания, а в некоторые времена и вовсе считалось богохульством.
Лишь в XVIII веке с развитием физики и химии, ученым удалось подтвердить и развить идеи Демокрита. Вот только простейшим представителем такого или иного вида метрии был уже не атом, а молекула. А вот молекула уже в свою очередь состоит из атомов.
Так, например, молекула воды H2O является мельчайшим представителем такого вещества как вода. А состоит молекула воды из двух атомов водорода и одного атома кислорода. Сами по себе водород и кислород не несут свойств воды. Наоборот, вода только и становится водой, когда образуется такая связь.
Итак, материя состоит из молекул. Но почему мы этого не замечаем? Ответ прост: молекулы так малы, что для человеческого глаза просто незаметны. Лишь только в электронные микроскопы можно рассмотреть отдельные молекулы.
Что меньше молекул?
Молекулы в свою очередь, как мы выяснили, состоят из атомов. Однако, в отличие от времен Демокрита, атомы больше не считаются неделимыми (что, впрочем, не помешало сохраниться названию). В начале XXвека ученым удалось "разрезать" атом и изучить внутреннее строение атома .
Выяснилось, что атом состоит из ядра и вращающегося вокруг ядра электрона. Позже выяснилось, что ядро в свою очередь состоит из протона и нейтрона. Физика XXIвека идет дальше и пытается выяснить, из чего же сделаны протоны, нейтроны и электроны. И те результаты, которых добиваются современные ученые, безусловно, порадовали бы Демокрита.
Роль Адронного Коллайдера в изучении строения вещества
Так, полным ходом идут эксперименты на Большом Адронном Коллайдере - огромном сооружение, построенном под землей на границе между Францией и Швейцарией. Большой Адронный Коллайдер представляет собой 30 километровую замкнутую трубу, по которой разгоняются протоны. Разогнавшись почти до скорости света, протоны сталкиваются.
Сила удара так велика, что протоны "разламываются" на части. Предполагается, что таким путем можно изучить внутреннее строение адронов (так называется протон, нейтрон или электрон). Очевидно, что чем дальше человек заходит в изучении внутреннего строения вещества, тем с большими трудностями он сталкивается.
Примечательно еще и то, что чем меньше размер искомой частицы, тем более массивное сооружение для изучения необходимо построить. Ирония, однако... Не исключено, что неделимой частицы, которую воображал себе Демкорит, вообще не существует и делить частицы можно до бесконечности. Исследования в данной области являются одной из самых бурно развивающихся тем в современной физике.
По современным представлениям:
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Неправильно говорить, что «атом – наименьшая частица химического элемента, сохраняющая все его химические свойства», т. к. химический элемент – это вид частиц (атомов, ионов, ядер) с определенным зарядом ядра; поэтому элемент не состоит из атомов!
Кроме того, химические свойства – это энергетика и скорость химической реакции, а они зависят не только от состава реагирующей частицы, но и от ее энергетического состояния, геометрической формы и т. п., потому химическими свойствами обладают не атомы (и молекулы), а их совокупности – химические вещества.
Молекула – это электронейтральная наименьшая совокупность атомов, образующих определенную структуру посредством химических связей, определяющая состав вещества.
Согласно современным представлениям из молекул состоят вещества в газо- и парообразном состоянии. В твердом состоянии из молекул состоят лишь вещества, кристаллическая решетка которых имеет молекулярную структуру (большинство органических веществ; неметаллы, кроме бора, кремния, аллотропных модификаций углерода; углекислый газ СО 2 ; вода Н 2 О).
Большинство же твердых неорганических веществ не имеет молекулярной структуры: их решетка состоит не из молекул, а из других частиц (ионов, атомов); они существуют в виде макротел (кристалл NaCl, друза кварца, кусок железа и др.). К веществам немолекулярного строения относятся соли, оксиды металлов, алмаз, кремний, металлы и др.
Химическая связь между молекулами у веществ с молекулярной структурой менее прочная, чем между атомами в молекуле, поэтому их температуры плавления и кипения сравнительно низкие. У веществ с немолекулярной структурой химическая связь между частицами весьма прочная, поэтому их температуры плавления и кипения высокие.
1.3.2. Массы атомов и молекул. Моль
Массы атомов и молекул чрезвычайно малы, поэтому для них используют специальную единицу измерения – атомную единицу массы (сокращенное обозначение «а. е. м.»):
1 а. е. м. = 1,66·10 –27 кг.
Например, абсолютная масса атома алюминия:
m o (Al) = 4,482·10 –26 кг = 27 а. е. м.
Чаще используют безразмерные величины – относительные атомные и молекулярные массы.
Относительная атомная масса A r – число, показывающее, во сколько раз масса данного атома больше 1/12 массы атома углерода 12 С.
Например:
A r (Al) = = 27.
Относительная молекулярная масса M r – число, показывающее, во сколько раз масса данной молекулы больше 1/12 массы атома углерода 12 С.
Например:
M r (SO 2)
=
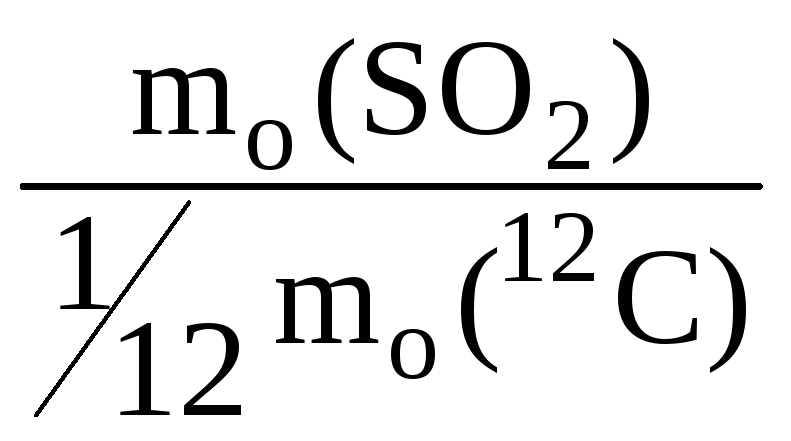 = 64.
= 64.
Наряду с единицами массы и объема, в химии пользуются также единицей количества вещества, называемой молем (сокращенное обозначение – «моль»).
Моль – это количество вещества, содержащее столько же структурных единиц (атомов, молекул, ионов, ядер, электронов, радикалов), сколько содержится атомов в 0,012 кг (12 г) углерода 12 C.
В одном моле любого вещества содержится число Авогадро структурных единиц, а именно
N A = 6,02·10 23 моль –1 .
Моль вещества имеет определенную массу (молярную массу) и определенный объем (молярный объем).
Молярная (мольная) масса М – это масса 1 моль вещества, выраженная в единицах массы:
M(Al) = 27 г/моль; M(H 2 SO 4) = 98 г/моль.
Молярный (мольный) объем V m – объем 1 моль вещества, выраженный в единицах объема:
V m (CO 2) = 22,4 л/моль (н. у.) 1 ; V m (H 2 O) = 18 мл/моль.
Пример 1.1 . Во время войны во Вьетнаме (1962–1971 гг.) американские войска широко использовали дефолианты в борьбе с партизанами. Дефолиант «agent orange» (оранжевый реактив) вызывает ускоренное опадание листьев деревьев. Всего над джунглями было распылено 57 тыс. т этого препарата, в котором в виде примеси содержалось до 170 кг диоксина. Сейчас этот дефолиант известен под названием 2,4-D (2,4-дихлорфеноуксусная кислота).Рассчитайте массу одной молекулы дефолианта (молекулярная формула С 8 Н 6 O 3 Cl 2): а) в граммах; б) в атомных единицах массы.
Решение:
а). Для расчета массы молекулы 2,4-дихлорфеноуксусной кислоты необходимо знать ее молярную массу:
М(С 8 Н 6 O 3 Cl 2) = 8 · 12 + 6 · 1 + 3 · 16 + 2 · 35,5 = 221 (г/моль).
Рассчитываем количество вещества по следующим формулам:
ν = m / M; ν = N / N A ,
где m – масса, M – молярная масса, N – число атомов или молекул, N A = 6,02·10 23 моль –1 – постоянная Авогадро.
Объединив эти формулы можно выразить массу через число молекул:
m
= ν
· M
=
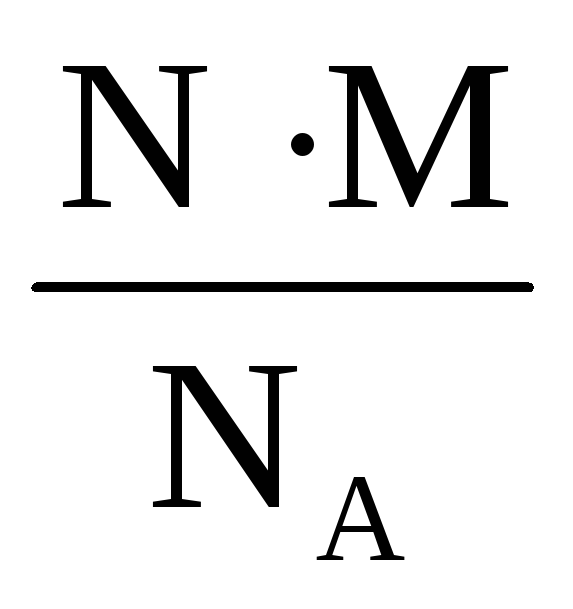 .
.
Подставляя в полученную формулу N = 1, M = 221 г/моль, N A , находим:
m(С 8 Н 6 O 3 Cl 2)
=
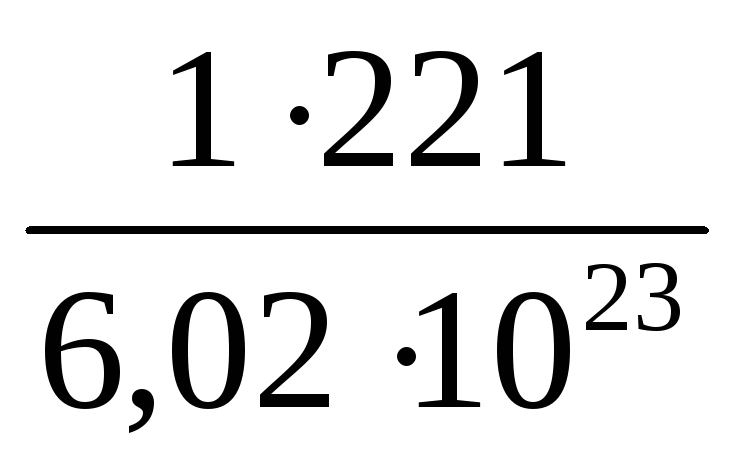 =
36,7·10 –23
(г).
=
36,7·10 –23
(г).
б). Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на 1 а. е. м.
m(С 8 Н 6 O 3 Cl 2) = 1 а. е. м. · M r (С 8 Н 6 O 3 Cl 2)
Относительная молекулярная масса численно равна молярной массе:
M r (С 8 Н 6 O 3 Cl 2) = 221;
m(С 8 Н 6 O 3 Cl 2) = 1 а. е. м. · 221 = 221 а. е. м.
Пример 1.2. Сколько молекул содержится в 1 л воды?
Решение. 1. Массу 1 л воды можно вычислить, используя величину плотности (плотность воды при 4С равна 1 г/см 3):
m(H 2 O) = V(H 2 O) · ρ(H 2 O);
V(H 2 O) = 1 л = 1 дм 3 = 1000 см 3 ;
m(H 2 O) = 1000 см 3 · 1 г/см 3 = 1000 г.
2. Дальнейшие рассуждения можно вести двумя способами.
1 способ: по количеству вещества.
Пользуясь формулами ν = m / M и ν = N / N A , находим:
ν(Н 2 О) = m(Н 2 О) / M(Н 2 О); ν(Н 2 О) = 1000 г / 18 г/моль = 55,6 моль.
N(H 2 O) = ν(Н 2 О) · N A ; N(H 2 O) = 55,6 моль · 6,02·10 23 моль –1 = 334,7·10 23 = 3,35·10 25 .
2 способ: с помощью пропорции.
18 г (1 моль) H 2 O содержат 6,02·10 23 молекул;
1000 г Н 2 О содержат N молекул.
N(H 2 O) = 1000 · 6,02·10 23 / 18 = 3,35·10 25 .
Пример 1.3. Вычислите молярный объем алюминия, если его плотность составляет 2,7 г/см 3 .
Решение. Для вычисления молярного объема через плотность вещества необходимо знать его молярную массу:
ρ(Al)
=
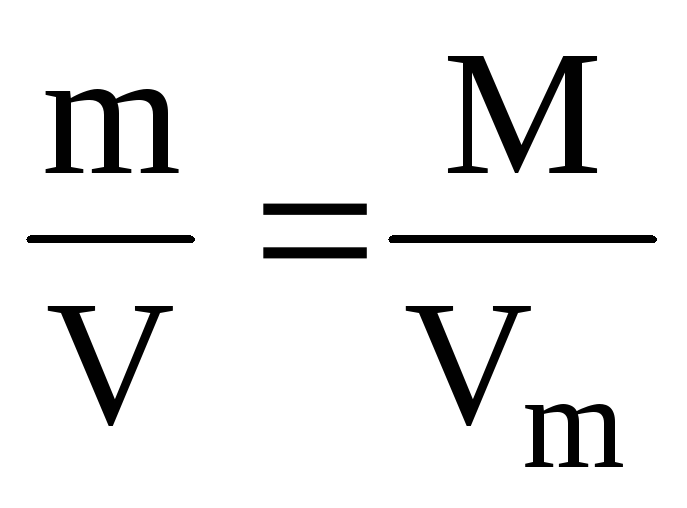 ;V m (Al)
=
;V m (Al)
=
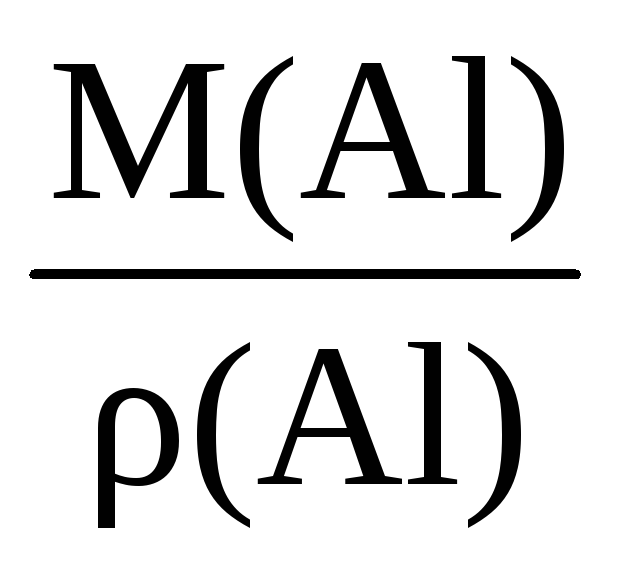 .
.
V m (Al)
=
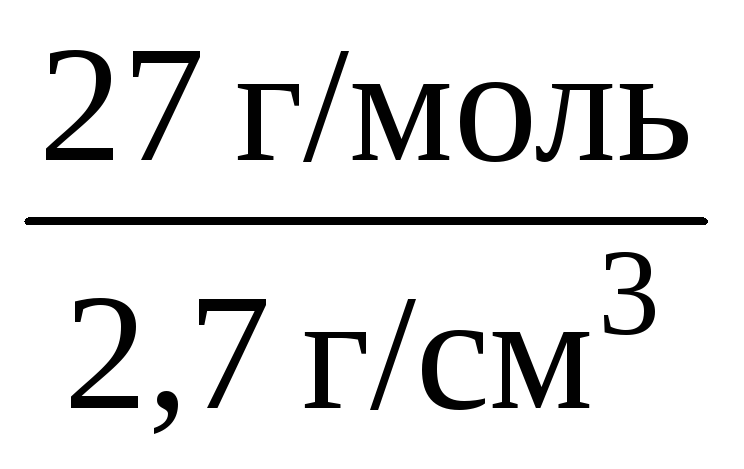 = 10 см 3 /моль
= 0,01 л/моль.
= 10 см 3 /моль
= 0,01 л/моль.













