Сложные молекулы примеры. Молекулярные вещества
Урок №6. Атомы и молекулы. Атомно – молекулярное учение. Вещества молекулярного и немолекулярного строения
I. Новый материал
Эта лекция будет посвящена следующим понятиям: "атом", "молекула", "вещества молекулярного и немолекулярного строения", "атомно-молекулярное учение".
Возникновение представлений об атомах и молекулах
Древнегреческий 2500 лет назад высказал мысль о том, что все тела в природе состоят из мельчайших невидимых, непроницаемых, неделимых, вечно движущихся частиц – атомов. Слово “атом” в переводе означает “неделимый”. Позднее, в средние века, учение об атомах преследовалось религией, которая тормозила развитие науки в целом, и химии в частности.
Учение о молекулах и атомах было разработано в середине 18 века великим русским ученым (1711 – 1765 гг.) Он утверждал, что тела в природе состоят из корпускл (молекул), в состав которых входят элементы (атомы). Многообразие веществ ученый прозорливо объяснял соединением разных атомов в молекулах и различным расположением атомов в них. Удивительно верной и смелой для того времени была мысль М. В. Ломоносова о том, что некоторые корпускулы (молекулы) могут состоять из одинаковых элементов (атомов). Учение об атомах получило дальнейшее развитие в трудах известного английского ученого (1766 – 1844 гг.).
МОЛЕКУЛЫ И АТОМЫ
Можно ли опытным путем доказать, что молекулы состоят из атомов?
То, что атомы действительно существуют, подтверждают многие химические реакции. Так, например, при пропускании постоянного тока через воду в одной из трубок прибора собирается газ, в котором тлеющая лучинка ярко вспыхивает. Это кислород. В другой трубке собирается вдвое больше газа, который от зажженной лучинки загорается. Это водород.
Схема аппарата для разложения воды (аппарат Гофмана)
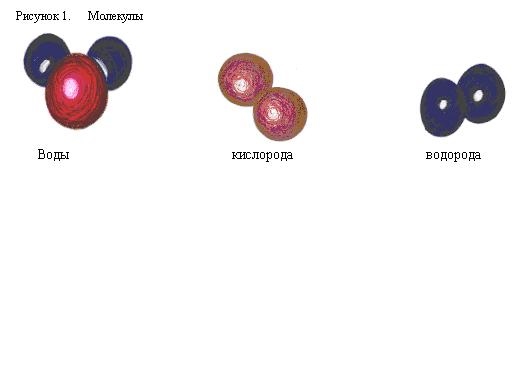
Объяснить это явление можно так. Мельчайшая частица воды – молекула состоит из 2 атомов водорода и одного атома кислорода. При пропускании постоянного тока через воду ее молекулы распадаются и образуются химически неделимые частицы – атомы кислорода и водорода. Затем атомы соединяются по два, и из двух молекул воды образуется одна – двухатомная молекула кислорода и две водорода.
Некоторые представления об атомах и молекулах, высказанные М. В. Ломоносовым за полвека до Д. Дальтона, оказались более достоверными и научными. Например, английский ученый категорически отрицал возможность существования молекул, состоящих из одинаковых атомов. Его взгляды отрицательно сказались на развитие химии. Учение о молекулах и атомах окончательно было принято только в 1860 г. на Всемирном съезде химиков в Карлеруэ.
Итак, что такое молекулы и атомы?
Молекулы – мельчайшие частицы вещества, состав которых и химические свойства такие же, как у данного вещества. Молекулы – предельный результат механического дробления вещества.
Атомы – это мельчайшие химически неделимые частицы, из которых состоят молекулы. Молекулы, в отличие от атомов, являются химически делимыми частицами.
Молекулярные вещества молекулы
Молекулы - наименьшая частица молекулярного вещества, способная существовать самостоятельно и сохраняющая его химические свойства.
Молекулярные вещества имеют низкие температуры плавления и кипения и находятся в стандартных условиях в твердом, жидком или газообразном состоянии.
Например: Вода - жидкость, t пл =0°С; t кип =100°С
Вода – самое известное и весьма распространенное вещество на нашей планете: поверхность Земли на
3
/
4
покрыта водой, человек на 65 % состоит из воды, без воды невозможна жизнь, так как в водном растворе протекают все клеточные процессы организма. Вода – молекулярное вещество. Это одно из немногих веществ, которое в природных условиях встречается в твердом, жидком и газообразном состояниях, и единственное вещество, для которого в каждом из этих состояний есть свое название.
Особенностями строения воды вызваны ее необычные свойства. Например, при замерзании вода увеличивается в объеме, поэтому лед плавает в своем расплаве – жидкой воде, а наибольшая плотность воды наблюдается при 4
o
С, поэтому зимой большие водоемы до дна не промерзают. На свойствах воды основана и сама шкала температур Цельсия (0
o
– температура замерзания, 100
o
– температура кипения). С причинами этих явлений и с химическими свойствами воды вы познакомитесь позже.
Немолекулярные вещества
Немолекулярные вещества - это вещества, мельчайшими структурными частицами которых являются атомы или ионы .
Ион - это атом или группа атомов, обладающих положительным или отрицательным зарядом.
Например: Na + , Cl - .
Немолекулярные вещества находятся в стандартных условиях в твердом агрегатном состоянии и имеют высокие температуры плавления и кипения.
Например: Поваренная соль - твердое вещество, t пл =801°С; t кип =1465°С; Железо
Железо – серебристо-белый, блестящий, ковкий металл. Это немолекулярное вещество. Среди металлов железо занимает второе место после алюминия по распространенности в природе и первое место по значению для человечества. вместе с другим металлом – никелем – оно образует ядро нашей планеты. Чистое железо не имеет широкого практического применения. Знаменитая Кутубская колонна, расположенная в окрестностях Дели, высотой около семи метров и весом 6,5 т, имеющая возраст почти 2800 лет (она поставлена в IX в. до н. э.) – один из немногих примеров использования чистого железа (99,72 %); возможно, что именно чистотой материала и объясняется долговечность и коррозионная устойчивость этого сооружения.

В виде чугуна, стали и других сплавов железо используется буквально во всех отраслях техники. Его ценные магнитные свойства используются в генераторах электрического тока и электромоторах. Железо является жизненно необходимым элементом для человека и животных, так как оно входит в состав гемоглобина крови. При его недостатке клетки тканей получают недостаточно кислорода, что ведет к очень тяжелым последствиям.
Атомно-молекулярное учение
Атомно-молекулярное учение развил и впервые применил в химии великий русский ученый Ломоносов. Сущность учения Ломоносова можно свести к следующим положениям.
1. Все вещества состоят из «корпускул» (так Ломоносов называл молекулы).
2. Молекулы состоят из «элементов» (так Ломоносов называл атомы).
3. Частицы - молекулы и атомы - находятся в непрерывном движении. Тепловое состояние тел есть результат движения их частиц.
4. Молекулы простых веществ состоят из одинаковых атомов, молекулы сложных веществ - из различных атомов.
Атомистическое учение в химии применил английский ученый Джон Дальтон. В своей основе учение Дальтона повторяет учение Ломоносова. Вместе с тем оно развивает его дальше, поскольку Дальтон впервые пытался установить атомные массы известных тогда элементов. Однако Дальтон отрицал существование молекул у простых веществ, что по сравнению с учением Ломоносова является шагом назад. По Дальтону, простые вещества состоят только из атомов, и лишь сложные вещества - из «сложных атомов» (в современном понимании - молекул). Отрицание Дальтоном существования молекул простых веществ мешало дальнейшему развитию химии. Атомно-молекулярное учение в химии окончательно утвердилось лишь в- середине XIX в.Молекула - это наименьшая частица данного вещества, обладающая его химическими свойствами. Химические свойства молекулы определяются ее составом и химическим строением. Атом - наименьшая частица химического элемента, входящая в состав молекул простых и сложных веществ. Химические свойства элемента определяются строением его атома. Отсюда следует определение атома, соответствующее современным представлениям: атом - это электронейтральная частица, состоящая из положительно заряженного атомного ядра и отрицательно заряженных электронов. Согласно современным представлениям из молекул состоят вещества в газообразном и парообразном состоянии. В твердом состоянии из молекул состоят лишь вещества, кристаллическая решетка которых имеет молекулярную структуру.
Основные положения атомно-молекулярного учения можно сформулировать так:
Существуют вещества с молекулярным и немолекулярным строением.
Между молекулами имеются промежутки, размеры которых зависят от агрегатного состояния вещества и температуры. Наибольшие расстояния имеются между молекулами газов. Этим объясняется их легкая сжимаемость. Труднее сжимаются жидкости, где промежутки между молекулами значительно меньше. В твердых веществах промежутки между молекулами еще меньше, поэтому они почти не сжимаются.
Молекулы находятся в непрерывном движении. Скорость движения молекул зависит от температуры. С повышением температуры скорость движения молекул возрастает.
Между молекулами существуют силы взаимного притяжения и отталкивания. В наибольшей степени эти силы выражены в твердых веществах, в наименьшей - в газах.
Молекулы состоят из атомов, которые, как и молекулы, находятся в непрерывном движении.
Атомы одного вида отличаются от атомов другого вида массой и свойствами.
При физических явлениях молекулы сохраняются, при химических, как правило, разрушаются.
У веществ с молекулярным строением в твердом состоянии в узлах кристаллических решето находятся молекулы. Связи между молекулами, расположенными в узлах кристаллической решетки, слабые и при нагревании разрываются. Поэтому вещества с молекулярным строением, как правило, имеют низкие температуры плавления.
У веществ с немолекулярным строением в узлах кристаллических решеток находятся атомы или другие частицы. Между этими частицами существуют сильные химические связи, для разрушения которых требуется много энергии. Поэтому вещества с немолекулярным строением имеют высокие температуры плавления.
Объяснение физических и химических явлений с точки зрения атомно-молекулярного учения. Физические и химические явления получают объяснение с позиций атомно-молекулярного учения. Так, например, процесс диффузии объясняется способность молекул (атомов, частиц) одного вещества проникать между молекулами (атомами, частицами) другого вещества. Это происходит потому, что молекулы (атомы, частицы) находятся в непрерывном движении и между ними имеются промежутки. Сущность химических реакций заключается в разрушении химических связей между атомами одних веществ и в перегруппировке атомов с образованием других веществ.
II. Закрепление
Дайте ответы на следующие вопросы:
Назовите имя древнегреческого философа, который высказал мысль о том, что все тела в природе состоят из мельчайших невидимых, непроницаемых, неделимых, вечно движущихся частиц – атомов.
Назовите имя великого русского учёного, основоположника учения о молекулах и атомах.
Дайте определение молекуле.
Дайте определение атому.
Какие вещества относят к веществам молекулярного строения? Приведите примеры веществ.
Какие вещества относят к веществам немолекулярного строения? Приведите примеры веществ.
Какими свойствами характеризуются веществамолекулярного строения?
Какими свойствами характеризуются веществанемолекулярного строения?
Как объяснить физические и химические явления с точки зрения атомно-молекулярного учения?
МОЛЕКУЛА
(новолат.
molecula, уменьшит. от лат. moles-масса), микрочастица, образованная из двух
или большего числа и способная к самостоят. существованию. Имеет постоянный
состав (качеств. и количеств.) входящих в нее и фиксир. число
и обладает совокупностью св-в, позволяющих отличать одну молекулу от других, в т.
ч. от молекул того же состава. Молекула как система, состоящая из взаимодействующих
и ядер, может находиться в разл. состояниях и переходить из одного состояния
в другое вынужденно (под влиянием внеш. воздействий) или самопроизвольно. Для
всех молекул данного вида характерна нек-рая совокупность состояний, к-рая может
служить для молекул. Как самостоят. образование молекула обладает в каждом
состоянии определенным набором физ.
св-в, эти св-ва в той или иной степени сохраняются при переходе от молекул к состоящему
из них в-ву и определяют св-ва этого в-ва. При хим. превращениях молекулы одного в-ва
обмениваются с молекулами др. в-ва, распадаются на молекулы с меньшим числом ,
а также вступают в хим. р-ции др. типов. Поэтому изучает в-ва и их превращения
в неразрывной связи со строением и состоянием молекул.
Обычно молекулой наз. электрически
нейтральную частицу; если молекула несет электрич. заряд (положит. или отрицат.),
то говорят о мол. ( или соотв.). В в-ве положит.
всегда сосуществуют вместе с отрицательными. Молекулы, находящиеся в состояниях с
мультиплетпостью, отличной от единицы (как правило, в дублетных состояниях),
наз. радикалами. Своб. радикалы в обычных условиях, как правило, не могут существовать
длит. время. Известны, однако, своб. радикалы сравнительно сложного строения,
к-рые являются достаточно стабильными и могут существовать при обычных условиях
(см. ).
По числу входящих в молекулу
различают молекулы двухатомные, трехатомные и т.д. Если число
в молекуле превосходит сотни и тысячи, молекуле наз. . Сумма масс всех
, входящих в состав молекулы, рассматривается как (см.
также , ). По
величине мол. массы все в-ва условно делят на низко- и высокомолекулярные.
Классическая
рассматривает молекулу как стабильную наименьшую (по массе
и размерам) частицу в-ва, определяющую его основные св-ва. Эта частица образована
из химически связанных друг с другом (одинаковых или разных). Понятие
в молекуле при этом не детализируется; он, вообще говоря, отличается от изолир.
, так что говорят об эффективном , поведение и св-ва к-рого различны
в разных молекулах.
Из всех возможных взаимод.
в молекулах выделяют главные взаимод., или , к-рые обеспечивают
стабильное существование молекулы и сохранение ею своих основных характеристик в достаточно
широкой области изменения внеш. условий. Все прочие (неглавные) взаимод. между
в молекуле не определяют ее существования как целого, хотя и влияют, подчас
значительно, на те или иные св-ва. О неглавных взаимод. говорят как о взаимном
влиянии непосредственно не связанных , или .
Энергетически главные взаимод. в данной молекуле, как правило, более значительны,
чем неглавные. Вопрос о том, является ли взаимод. выделенной в молекуле
главным или неглавным, решается на анализа многих физ. и физ.-хим.
св-в в-ва, образованного из этих молекул.
Квантовомеханическая
теория
представляет молекулу как систему, состоящую из и
и находящуюся в определенном , из к-рого молекула может
перейти в др. . Каждое состояние и его изменение во времени
() определяется либо волновой ф-цией, к-рую находят как решение ур-ния
Шрё-дингера (стационарного или временного), либо , удовлетворяющей
квантовому ур-нию Лиувилля (см. ). Для изолированных
молекул ур-ние Шрёдингера решается обычно в такой системе координат, начало к-рой
находится в центре масс (молекулы или системы ). Это позволяет отделить
поступат. движение молекулы от всех др. видов движений. Для стационарного состояния
изолированной молекулы волновая ф-ция либо существенно локализована в нек-рой конечной
области пространства и описывает связанное (связное, стабильное) состояние системы
, либо такой локализацией не обладает, описывая отталкивательное
(несвязанное) состояние системы. В отталкиват. состоянии молекулы как таковой фактически
нет, а есть ее фрагменты, взаимодействующие друг с другом, на к-рые молекула, будучи
переведенной в такое состояние, распадается. Возможны и нестационарные состояния
молекулы, к-рые, однако, меняются во времени настолько медленно, что
молекула может находиться в этих состояниях достаточно длительно (в сравнении с характеристич.
временем эксперимента или временем наблюдения за системой). Подобные состояния
молекулы обычно наз. метастабильными (или квазисвязанными).
Для изолированной молекулы направления
осей системы координат, начало к-рой находится в центре масс, выбираются так,
чтобы по возможности полнее исключить из рассмотрения вращение молекулы как
целого (напр., оси координат м. б. направлены по главным осям эллипсоида инерции
молекулы или связаны с к.-л. выделенной конфигурацией ядер). Согласно , для каждой фик-сир. конфигурации можно определить
электронное состояние и соответствующие ему электронную волновую ф-цию и собств.
значение электронного гамильтониана - электронную энергию (см. ). Электронная энергия Е e зависит от набора переменных
R, определяющих конфигурацию ядер. Она включает потенциал межъядерного
отталкивания и изображается графически
Е е = Е е {R} (или просто потенц. пов-стью)
молекулы в данном электронном состоянии. В частности, для двухатомных молекул электронная
энергия изображается потенц. кривой Е e = E e (R), где
R -расстояние между ядрами .
Потенц. пов-сть наглядно
представляет тот потенциал, в к-ром движутся ядра рассматриваемой молекулы; решениями
ур-ния Шрёдингера с этим потенциалом являются колебат. волновые ф-ции, квадрат
модуля к-рых определяет плотность вероятности обнаружить у данной молекулы ту или
иную ядерную конфигурацию. Потенц. пов-сть для молекулы, находящейся в связанном электронном
состоянии, м. б. достаточно простой, напр. иметь один минимум, отвечающий т.
наз. равновесной геом. конфигурации ядер. При увеличении межъядерных расстояний
потенц. энергия молекула увеличивается до определенного предельного значения, при
к-ром молекула диссоциирует на два (или большее число) мол. фрагмента (напр., ).
Для многоатомных молекул потенц. пов-сти обычно имеют более сложный вид с неск. локальными
минимумами, разделенными потенц. барьерами, а также с точками перевала, разл.
долинами, складками и т. п. К тому же потенц. пов-сти для разл. электронных
состояний молекулы могут достаточно близко подходить друг к другу, пересекаться, совпадать
в отдельных точках. В таких областях подчас невозможно использовать адиабатич.
приближение и наглядная картина изменения состояний молекулы как движений по потеиц.
пов-сти утрачивается. Если колебат. волновая ф-ция, характеризующая плотность
распределения ядер, локализована вблизи к.-л. минимума на потенц. пов-сти, причем
по энергии этот минимум лежит ниже диссоциац. пределов для данной молекулы, то можно
говорить о наличии у молекулы в рассматриваемом электронно-колебат. состоянии структурного
с равновесной конфигурацией, отвечающей минимуму потенц. энергии. Разным
минимумам, если они не переводятся обычными операциями друг в друга,
соответствуют разные структурные , причем большая или меньшая легкость
перевода одного в другой определяется потенц. барьерами, к-рые разделяют
эти минимумы. Так, н-бутан и в основном электронном состоянии,
с точки зрения квантовомех. теории, суть одна и та же молекула С 4 Н 10 ,
на потенц. пов-сти к-рой имеются по крайней мере два минимума: один-абс. минимум,
к-рому отвечает равновесная конфигурация изо-бутана, и второй-локальный минимум,
к-рому отвечает равновесная конфигурация н-бутана. Вероятность спонтанного
перехода из потенц. ямы вблизи одного минимума в потенц. яму вблизи др. минимума
для низших колебат. состояний очень мала, что и определяет раздельное существование
молекул н-бутана и .
В др. случаях на потенц.
пов-сти имеются минимумы, разделенные сравнительно невысокими барьерами (от
неск. десятых до неск. кДж/), либо пологие долины или желоба, при движении
вдоль к-рых энергия молекулы меняется примерно в тех же пределах. Так, у NaAlF 4
имеется четыре
эквивалентных
минимума, разделенных невысокими барьерами. Минимумы отвечают симметричной координации
Na у каждой из четырех граней тетраэдра AlF 4 (тридентантная координация);
каждый из барьеров отвечает геом. конфигурации ядер с координацией Na у ребра
тетраэдра AlF 4 (бидентантная координация). Na может относительно
свободно перемещаться вокруг тетраэдрич. остова. Подобные молекулы получили название
политопич. молекул, или молекул с распределенным характером связи. У KCN К может
относительно свободно перемещаться по желобу потенц. пов-сти вокруг остова CN,
так что в одних колебат. состояниях эта молекула имеет наиб. вероятную конфигурацию,
близкую к треугольной, в других-к линейной KNC, в третьих-к линейной KCN. Молекулы
такого типа, как и молекулы с распределенным характером связи, относятся к .
Полная волновая ф-ция молекулы
в определенном при использовании адиабатич. приближения
представляет собой произведение электронной волновой ф-ции на колебат. волновую
ф-цию. Если учесть и то, что молекула в целом вращается, в произведение войдет еще
один сомножитель - вращат. волновая ф-ция. Знание электронной, колебат. и вращат.
волновых ф-ций позволяет вычислить для каждого молекулы физически
наблюдаемые средние величины: средние положения ядер, а также средние межъядерные
расстояния и средние углы между направлениями от данного ядра к др. ядрам, в
т. ч. к ближайшим (); средние электрич. и магн. дипольные и , средние смещения электронного заряда при переходе от системы разделенных
к молекуле и др. Волновые ф-ции и энергии разл. состояний молекулы используют и для
нахождения величин, связанных с переходами из одного в
другое: частот переходов, вероятностей переходов, силы линий
и т. п. (см. ).
Если в систему ядер, образующих
молекулу, входят тождественные, то среди всех конфигураций ядер будут и такие, к-рые
обладают определенной пространств. . Потенц. пов-сти молекулы симметричны
относительно операций , к-рые отвечают таким конфигурациям. По этой
причине симметричные конфигурации ядер всегда отвечают экстремальным точкам
на потенц. пов-стях (минимумам, максимумам, точкам перегиба). Если равновесная
не обладает самой высокой , возможной для данной системы
ядер, или вовсе несимметрична, то должна быть и эквивалентная ей равновесная
конфигурация, получающаяся из исходной теми операциями , к-рые допускают
симметричные ядерные конфигурации данной молекулы (см. ).
Квантовая теория дает более
богатую и полную картину молекулы в ее разл. состояниях по сравнению с классич. теорией
хим. строения. Она позволяет прежде всего провести хим. связей
в молекулах на основе того или иного характера распределения
(ковалент-ные связи отвечают примерно симметричному распределению валентных между , образующими такие связи; отвечают сильному смещению этой плотности к одному из ), либо исходя
из представлений о происхождении той или иной связи (напр., ), либо по др. признакам (напр., молекула с сопряженными связями или молекула с распределенным
характером связи). Квантовая теория позволяет также учесть изменения состояний,
к-рые возникают при переходе от отдельной изолированной молекулы к в-ву, состоящему
из множества взаимодействующих друг с другом молекул при заданных внеш. условиях.
И хотя строгие исходные положения квантовой теории требуют, чтобы рассмотрение,
напр., двух взаимодействующих молекул (N 2 + N 2 , N 2
+ Н 2 О и т.п.) велось для единой системы, включающей все ядра и
этих двух молекул одновременно (в силу требований перестановочной для ,
подсистем тождеств. ядер и др.), все же методы квантовой теории позволяют во
мн. случаях сохранять представления об
отдельных
молекулах, возмущенных взаимным влиянием, но сохраняющих в значит. степени свою индивидуальность.
Таковы, в частности, представления
о молекулах (преим. с ко-валентными связями), сохраняющих при переходе в кон-денсир.
фазу в значит. степени равновесные межъядерные расстояния и валентные утлы,
осн. частоты колебаний и др. Подобные конденсир. фазы обычно наз. мол.
или мол. . С другой стороны, у молекул с индивидуальность
подчас не сохраняется и весь или представляет собой своего
рода единую молекулу. Как правило, сохраняют свои осн. характерные особенности и молекулы
в адсорбир. состоянии, а также в .
Отдельные молекулы в системе
приобретают смысл эффективных структурных фрагментов, аналогично эффективным
в молекулах в рамках классич. теории. В целом модель молекулы или системы взаимодействующих
молекул в квантовой теории по возможности строится обычно таким образом, чтобы сохранить
наглядные представления классич. теории.
Строение и свойства
молекул.
Классич. и квантовомех. теоретич. представления о молекулах подтверждаются и
уточняются обширным эксперим. материалом об их св-вах и связи этих св-в со строением.
Понятие включает при этом два аспекта: геом. строение равновесной
ядерной конфигурации в рассматриваемом состоянии (либо ядерной конфигурации,
усредненной по колебат. движению) и электронное строение, характеризуемое прежде
всего распределением при разл. геом. конфигурациях
ядер, изменением этого распределения при переходе от одной области ядерных конфигураций
к другой, а также распределением др. физ. величин (напр., двухэлектронной плотности).
Характеристиками геом. являются: д л и н ы с в я з е й (межъядерные
расстояния для , соединенных хим. связями), в а л е н т н ы е у г л ы
(углы между направлениями от данного ядра к ядрам двух соседних , соединенных
с рассматриваемым хим. связью), т о р с и о н н ы е, или д и-э д р а л ь н ы
е, у г л ы (двугранные углы между двумя плоскостями, проходящими через к.-л.
выделенные тройки ядер). Как правило, геом. аспект включает информацию о
входящих в молекулу , последовательности и кратности хим. связей между ними,
возможных конформац. и т.д. На основе классич. теории такое представление
о структуре молекул позволяет классифицировать близкие по строению структурные фрагменты
по типам, проводить корреляцию св-в молекул с числами имеющихся в них структурных
фрагментов определенных типов и сопоставлять св-ва молекул, построенных из однотипных
наборов структурных фрагментов. Наглядно при таком подходе молекулу в каждом состоянии
можно изобразить либо системой (колеблющихся) материальных точек, либо в общем
случае системой перекрывающихся сфер, радиусы к-рых задаются по определенным
правилам (см., напр., ).
Знание распределения дает возможность вычислить мн. св-ва при фиксир. ядерных конфигурациях
для каждого состояния, напр. электрич. св-ва ( , ), диа- и парамагнитные составляющие магн. восприимчивости
и т.п.
Объединение обоих аспектов
приводит к наиб. полному представлению о и его изменении при переходе
из одного состояния в другое, особенностях отдельных классов и гомологич.
рядов и их поведении во внеш. полях и при взаимод. друг с другом.
Спектроскопич. методы основаны на индивидуальности спектров хим. соединений, к-рая обусловлена характерным для каждой молекулы набором состояний и отвечающих им энер-гетич. уровней. Эти методы позволяют проводить качественный и количественный в-в. Спектры поглощения или испускания в микроволновой области спектра позволяют изучать переходы между вращат. состояниями, определять моменты инерции молекул, а на их основе-длины связей, и др. геом. параметры молекул. исследует, как правило, переходы между колебательно-вращат. состояниями и широко используется для спектрально-аналит. целей, поскольку мн. частоты колебаний определенных структурных фрагментов молекул являются характеристическими и слабо меняются при переходе от одной молекулы к другой. В то же время позволяет судить и о равновесной геом. конфигурации (качественно-по соблюдению тех или иных в спектре, количественно - на основе решения обратной коле-бат. задачи, по крайней мере для малоатомных молекул; см.
Молекулярные вещества
Молекулярные вещества - это вещества, мельчайшими структурными частицами которых являются молекулы
Молекулы - наименьшая частица молекулярного вещества, способная существовать самостоятельно и сохраняющая его химические свойства. Молекулярные вещества имеют низкие температуры плавления и кипения и находятся в стандартных условиях в твердом, жидком или газообразном состоянии.
Wikimedia Foundation . 2010 .
Смотреть что такое "Молекулярные вещества" в других словарях:
Спектры испускания, поглощения и комбинационного рассеяния света (КРС), принадлежащие свободным или слабо связанным между собой молекулам. Типичные М. с. полосатые, они наблюдаются в виде совокупности более или менее узких полос в УФ, видимой и… … Физическая энциклопедия
Направленные потоки молекул или атомов, движущихся в вакууме практически без столкновения друг с другом и с молекулами остаточных газов. М. и а. п. позволяют изучить свойства отд. ч ц, пренебрегая эффектами, обусловленными столкновениями, кроме… … Физическая энциклопедия
Кристаллы, образованные из молекул, связанных друг с другом слабыми ван дер ваальсовыми силами (см. Межмолекулярное взаимодействие) или водородной связью. Внутри молекул между атомами действует более прочная ковалентная связь. Фазовые превращения … Википедия
Кристаллы, образованные из молекул, связанных друг с другом слабыми ван дер ваальсовыми силами или водородной связью (см. МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ, МЕЖАТОМНОЕ ВЗАИМОДЕЙСТВИЕ). Внутри молекул между атомами действует более прочная, обычно… … Физическая энциклопедия
Большой Энциклопедический словарь
МОЛЕКУЛЯРНЫЕ КРИСТАЛЛЫ,. кристаллы, в узлах кристаллической решетки которых располагаются молекулы вещества, связанные друӠс другом слабыми или ван дер ваальсовыми силами (см. МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ) или водородной связью (см. ВОДОРОДНАЯ… … Энциклопедический словарь
Вещества поверхностноактивные анионоактивные - Вещества поверхностно активные анионовоактивные – разновидность поверхностноактивных веществ; представляют собой высоко молекулярные органические кислоты (нафтеновые, сульфонафтеновые и др.), соли щелочноземельных и тяжелых металлов,… … Энциклопедия терминов, определений и пояснений строительных материалов
Микропористые тела, избирательно поглощающие из окружающей среды вещества, размеры молекул которых меньше размеров микропор. К ним относятся природные и синтетические цеолиты. Молекулярные сита позволяют производить адсорбционное разделение… … Энциклопедический словарь
Оптические спектры испускания, поглощения и рассеяния света, принадлежащие свободным или слабо связанным молекулам. Состоят из спектральных полос и линий, структура и расположение которых типичны для испускающих их молекул. Возникают при… … Энциклопедический словарь
Книги
- Полимеризация , Джесси Рассел. Эта книга будет изготовлена в соответствии с Вашим заказом по технологии Print-on-Demand. High Quality Content by WIKIPEDIA articles! Полимериза?ция (др.-греч. ????????? - состоящий из…
Cтраница 3
Приведите примеры молекул, которые содержат: а) только а-связи; б) одну а - и одну я-связи; в) две ст - и одну я-связи; г) две о - и две я-связи; д) одну а - и две л-связи; е) три а - и одну я-связи; ж) четыре ст - и две я-связи.
Приведите примеры молекул (не менее 5), в которых степени окисления атомов и их валентности не совпадают.
На примере молекулы NO2 рассмотрим более подробно строение трехатомных молекул угловой формы с л - связями. В образовании молекулы NO2 принимают участие 2s -, 2px -, 2pv - к 2р2 - орбитали атома азота, 2рх -, 2ру - и 2pz - op - битали двух атомов кислорода. Из десяти атомных орбиталей образуются десять молекулярных орбиталей. Поскольку молекула NO2, как и Н2О, имеет угловую форму, то о-орбитали NO2 аналогичны а-орбиталям молекулы Н2О (с. В отличие от Н2О в молекуле NO2 за счет 2рг / - орбиталей азота и 2ру - орбиталей двух атомов кислорода образуются трехцентровые молекулярные л в - и яразр-орбитали.
На примере молекулы NO2 рассмотрим более подробно строение трехатомных молекул угловой формы с л-связями. В образовании молекулы NO2 принимают участие 2s -, 2рх -, 2ру - и 2рг - орбитали атома азота, 2рх -, 2ру - и 2pz - op - битали двух атомов кислорода. Из десяти атомных орбиталей образуются десять молекулярных орбиталей. Поскольку молекула N02, как и Н2О, имеет угловую форму, то о-орбитали NO2 аналогичны сг-орбиталям молекулы Н2О (с. В отличие от Н20 в молекуле N02 за счет 2ру - орбиталей азота и 2ру - орбиталей двух атомов кислорода образуются трехцентровые молекулярные я - и л разр-орбитали.
На примере молекул трех углеводородов - бутана, бутена-3 и бутадиена-1 3 - показаны формы их углеродных скелетов (рис. 59), соответствующих неравноценным минимальным запасам внутренней энергии их молекул. Как и отмечалось, вращение в бутене-3 вокруг связи С-С, соседствующей (но не сопряженной) со связью СС, осуществляется наиболее легко, что объясняет повышенную гибкость макромолекул каучуков, содержащих в своей цепи отдельные ненасыщенные группы.
На примере молекулы СО2 Ферми впэрвые показал, что такой резонанс приводит к возмущениям уровней анергии, весьма аналогичным колебательным возмущениям в спектрах двухатомных молекул (см. Молекулярные спектры I, гл. Единственное существенное различие состоит в том, что в двухатомных молекулах могут обладать близкой энергией и поэтому возмущать друг друга только колебательные уровни разных электронных состояний, тогда как в данном случае это может иметь место и для двух колебательных уровней одного и того же электронного состояния. В двухатомных молекулах причиной возмущения уровней является взаимодействие колебательного и электронного движения.
На примере молекулы хлоранила (рис. 362) видны отклонения в разные стороны от плоскости бензольного ядра валентно не связанных атомов хлора и кислорода.
На примере молекулы Н2 покажите, какие данные указывают на то, что при образовании связи происходит не касание, а перекрывание электронных облаков. Чем определяется глубина перекрывания.
На примере молекулы NH3 проверьте соблюдение первого уело - 1зия гр уппы, согласно которому произведение двух элементов симметрии есть элемент симметрии.
На примере молекулы бензола видно, что в методе резонанса порядок связи не является инвариантной величиной, а зависит от первоначального выбора резонирующих структур.