מרכיבים של מולקולת חלבון. פולאר חיובי חיובי. חמצון של חומצות שומן גבוהות יותר
חומרים מינרליים
קבוצת המאקרו-תזונתיים כוללת את אלה שתכולתם בחומר יבש משתנה מ -10% ל -10% n. אלה הם C, O, H, N, S ו- P, הכלולים בהרכב המולקולרי של חומרים בסיסיים, ו- Ca, Na, Cl, K, Mg, המהווים חלק ברקמות התומכות, דם, לימפה ורקמות אחרות.
קבוצת ultramicroelements כולל אלמנטים אשר התוכן שלהם הוא נמוך יותר מאשר n 10% -5 (Sb, Hg, Bi, Pb, וכו ').
זה כבר נקבע כי רוב האלמנטים הם biogenic, אשר הם בעלי חשיבות רבה להבטחת התפתחות נורמלית של תהליכי החיים הביוכימיים, החומרים המזינים החשובים ביותר כלולים IV (C); V (W, P) ו - VI (O, S) קבוצות של הטבלה המחזורית. אלמנטים VII (Cl, J, Mn) ו VIII (Fe, Co) קבוצות מעורבים היווצרות של חומרים בעלי ערך ביולוגי גבוה.
מרכיב אלמנט זכר של חומרי גלם תלוי בית גידול או צמיחה. בהתאם לריכוז של אלמנטים בודדים בסביבה ובאוכל, זמינותם, כמו גם יכולתם הסלקטיבית של סוגים מסוימים של אורגניזמים, משתנה גם מידת השימוש באלמנטים בודדים בתהליכי ההתבוללות.
סנאים
מבין החומרים האורגניים המרכיבים אורגניזמים חיים, המבנה הביולוגי החשוב ביותר והמורכב ביותר הוא חלבונים. כמעט כל ביטויי החיים (עיכול, עצבנות, התכווצות, צמיחה ורבייה, תנועה, מטבוליזם וכו ') קשורים בחומרים חלבוניים. לחלבונים יש תפקיד חשוב בבניית החומר החי וביישום תהליכי פעילותו החיוניים.
זרזים ספציפיים של חלבון טבע - אנזימים - להאיץ תגובות כימיות המתרחשות בגוף. תרכובות חלבון שונות לבצע את התפקוד התחבורה, המספקים את הגוף עם חמצן וחומרים מזינים. הפירוק של 1 גרם של חלבון למוצרים הסופי מספק את הגוף עם אנרגיה של 4.27 קק"ל.
חלבונים מבודדים מאיברים ורקמות לתת משקע לבן כאשר מחומם יש את אותם תכונות פיזיות כמו חלבון ביצה עוף. לכן, הם החלו להיקרא סנאים. מילה נרדפת למילה "חלבון" היא המילה "חלבון" (מן החלבונים היוונית - הראשון, הראשי).
חלבונים הם פולימרים מולקולריים גבוהים של חומצות אמינו שונות. בתרשים. 1 מציג את הנוסחאות של חומצות אמינו שונות.
איור 1. נוסחאות של כמה חומצות אמינו.
חומצות אמינו מחולקות לשתי קבוצות גדולות: חיוניות ולא ניתנות להחלפה. רוב חומצות האמינו נוצרות בגוף של בעלי חיים ובני אדם כתוצאה הידרוליזה של חלבונים מזון ביוסינתזה. אבל לפחות שמונה חומצות אמינו אינן מסונתזות בגוף. אלה valine, leucine, isoleucine, threonine, lysine, פנילאלנין, טריפטופן ו methionine, נקרא שאין לו תחליף. חלבונים חסרים אחד או יותר של חומצות אמינו אלה נקראים ביולוגית חסר. חלבוני בעלי חיים, כולל חלבונים hydrobiont, מכילים את כל חומצות האמינו החיוניות.
חומצות האמינו המרכיבות את החלבון מקושרות יחד על ידי קשרי פפטידים, אשר נוצרים בין הקבוצה האמינית של חומצת אמינו אחת לבין קבוצת הקארבוקסיל של האחר. המנגנון של תהליך זה מוצג באיור. 2
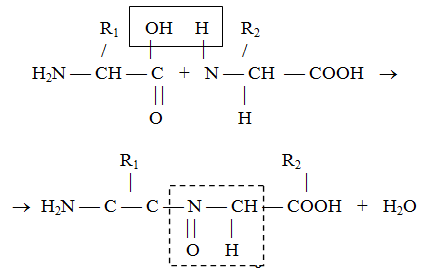
איור. 2. היווצרות המבנה העיקרי של החלבון.
פוליפפטידים וכתוצאה מכך הם הבסיס של כל החלבונים, ואת רצף מסוים של חומצות אמינו מוטבע בהם מאפיין את המבנה העיקרי של החלבון.
לכן, מאז מקרומולקולות חלבון בנויים ממאות רבות של חומצות אמינו, יש מספר אינסופי של האיזומרים שלהם בטבע, וכל סוג של יצור חי יכול להיות חלבון הטמון משלו.
שרשראות פוליפפטיד, בתורו, יכול להצטרף ליצירת מבנים חלבונים משניים, בעיקר בשל קשרים בין קבוצות שונות של פוליפפטידים. זה מוצג באופן סכמטי איור. 3
![]()
א) היווצרות של קשרי מימן
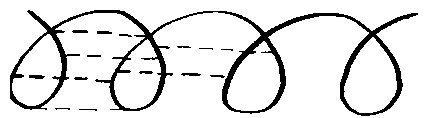
ב) היווצרות של סליל מן שרשרת פוליפפטיד
איור. 3. Scheme של היווצרות המבנה המשני של החלבון.
הסידור המרחבי של שרשרות הפוליפפטידים של מולקולת החלבון קובע את המבנה השלישני של מולקולת החלבון.
למעשה חלבונים - תרכובות מולקולריות גבוהות של מבנה מורכב, נבדלות הן פונקציות פיזיולוגיות תכונות כימיות. חלבונים של חומרי גלם מזון הם בעיקר במצב colloidal - בצורה של ג 'לים וסולס, אשר קובע מראש את חוסר היציבות ואת השתנות של תכונות (denaturation) של חומרים חלבונים כאשר התנאים הסביבתיים משתנים.
כאשר חומצת פתרונות חלבון ל pH של 4.5-5.0 (לדוגמה, במהלך כבישה), חלבונים לאבד את מסיסות שלהם להאיץ (קרישה). חלבונים רבים מאבדים את המסיסות שלהם כאשר פתרונות רוויים עם נתרן כלורי (כאשר מלוחים). בפרט, חלבונים שרירים עיקריים, מסיסים היטב בפתרונות של נתרן כלורי עם ריכוז של 7.5-10%, הם זירז (מלוחים החוצה) עם עלייה בריכוז שלה ל -15%. כאשר מחומם (במהלך בישול, צלייה, אפייה) חלבונים קרישה (קרישה). Denaturation תרמי של החלבונים מתחיל מ 28-35 ° C. Denaturation של חלבונים גם מתרחשת במהלך התייבשות (התייבשות) של המערכות שלהם (במהלך ייבוש והקפאה).
כאשר מזרז (המלחה החוצה, קרישה) חלבונים, הקשר שלהם עם מים מופרע.
כתוצאה מהמבנה הממדי התלת-ממדי "על פני השטח" של מולקולת החלבון הן קבוצות פעילות כימית - NH 2; -COOH; -. בפתרון מימי, קבוצות אלה נמצאים במצב מיונן עם האשמות של סימנים שונים. מולקולת חלבון רוכש סימן מתאים וגודל של תשלום בהתאם ליחס של קבוצות טעונות חיוביות ושליליות. המטען של מולקולת חלבון תלוי במצב שלה. כל שינוי במבנה של מולקולת חלבון מוביל לשינוי המטען שלה, בפרט, אובדן מוביל מוביל denaturation חלבון. הנוכחות של מטענים אלה גם קובע את תכונות ההידרציה של חלבונים. לדוגמה, מולקולה של מים מחוברת למולקולה חלבון חיובי חיובי עם הקצוות שלילית שלילית, ומבנה נוצר, שמרכזו הוא מולקולת חלבון, וסביב זה הוא קליפה monomolecular של מים. מאחר שכל הקצוות הטעונים שלילי של מולקולות המים הופכים למולקולת החלבון, אותו מטען נשאר על פני השטח של מבנה החלבון. בתורו, להצטרף לקבוצות חדשות של מולקולות מים, וכו '. באותו הזמן, שכבת hydrated מחובר אלקטרוסטטית נוצרת סביב כל מולקולת חלבון. עוצמת הקשר עם החלבון פוחתת ביחס למרווח המרחק מהמרכז, כלומר. ממולקולת החלבון, ובמרחק גדול מספיק בקנה מידה של גודלה של המולקולה, הקשר הזה כל כך קטן, כי התנועה התרמית של המולקולות מונעת פעולה של כוחות אלקטרוסטטיים. זה מגביל את כמות המים שמרו על פני השטח של החלבון.
על פי ההשקפות הקיימות, רקמת חלבונים יכולה להיחשב כגוף קולואיד קולואידאלי וקפילרי-נקבובי של מבנה מורכב מאוד, המבוסס על רשת מבנית של חלבונים נפוחים המכילים פתרונות צמיגיים המכילים חלבונים מסיסים וחומרים ניטרוגניים ומינרליים אחרים בעלי תכונות הידרופיליות. יחד עם זאת, חלק מהמים המהווים חלק מרקמת השריר מוחזק היטב על ידי חלבונים של הרשת המבנית, כמו גם מולקולות של חלבונים מומסים וחומרים הידרופיליים אחרים.
יחד עם המים המוחזקים על ידי שדה הכוח על פני השטח החיצוני והפנימי של חלקיקי חלבון, יש מים ברקמת השריר המוחזקת על ידי osmotically ועל ידי כוחות של צימוד מכני (מים נימי שמר). מים אלה נמצאים בנוזלים (תמיסות) המכילים חומרים ניטרוגניים ואורגניים שונים ומלחי מינרלים סגורים בתאים סגורים (micropores) בתוך מבני החלבון וחודרים את המיקרו-מקרופילרים. על פי נתוני הספרות, 1 גרם של חלבון נקשר בממוצע 0.3 גרם של מים כאשר hydrated.
כל שיטות העיבוד, המשטרים הטכנולוגיים מכוונים לשינוי המים ברקמות חומרי הגלם (רוויה במלח, הפיכתם לקרח, חימום לטמפרטורה הקרובה לנקודת הרתיחה, אידוי). שינוי באנרגיה הפנימית של המים מוביל לחוסר איזון בין החלבון והמים, אשר יוצר פגז לחות. מולקולת חלבון מגיב לכך על ידי ארגון מחדש המבנה שלה, ובהתאם לכך, על ידי שינוי גודל של החיוב. כאשר שינויים אלה הושלמו על ידי ירידה חדה או היעלמות מוחלטת של המטען, denaturation חלבון מתרחשת.
בהתאם עוצמת ומשך החשיפה החיצונית, denaturation חלבון יכול להיות הפיך, ללכת הפיך חלקית, או בלתי הפיך.
עומק denaturation ניתן לקבוע על ידי היכולת של רקמת שריר לשחזר באופן מלא או חלקי את הקשר עם מים.
המשמש כיום גבוהה חלבון עיבוד מזון שיטות להוביל בעיקר לשינויים, אשר יכול להיות מאופיין denaturation חלקית. ערכת denaturation של מולקולת חלבון מוצג באיור. 4
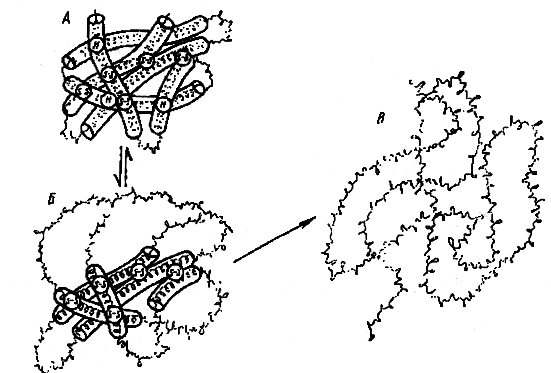
איור. 4. Scheme של denaturation של מולקולת חלבון:
A הוא המצב ההתחלתי, B הוא הפריסה הפיכה ההתחלתית, C הוא פריסה בלתי הפיכה מתקדמת.
השינויים האופייניים ביותר בחלבון במהלך denaturation תרמית (טמפרטורה 70-100 מעלות צלזיוס) הם אובדן של תכונות הילידים (היכולת להתמוסס במים, פתרונות של מלחים ואלכוהול), כמו גם ירידה ביכולת להתנפח.
השינויים בחלבון הקשורים denaturation תרמית הם גדולים יותר, גבוה יותר את הטמפרטורה ואת משך החימום, את ההשפעה של לחץ, ובתמיסה מימית החלבון denatures מהר יותר מאשר להיות במצב יבש.
לחלבון יש תפקיד חשוב במספר תהליכים טכנולוגיים: אפיית לחם, קונדיטוריה, ייבוש בשר, דגים, ירקות, חלב ואבקת ביצים, בייצור מזון משומר ועוד.
בתנאים של הבאת המוצר למוכנות מלאה, בדרך כלל עם חשיפה ממושכת לטמפרטורות קרוב ל 100 ° C, חלבונים עוברים שינויים נוספים הקשורים להרס של מקרומולקולות שלהם, הידרוליזה.
בתחילת התהליך, ניתן לנתק מוצרים נדיפים ממולקולות חלבון: דו תחמוצת הפחמן, מימן גופרתי, אמוניה, מימן זרחן וחומרים אחרים המעורבים בהיווצרות הטעם והניחוח של מוצרים מוגמרים. עם חשיפה ממושכת למים וחום, ההיווצרות של חומרים חנקניים מסיסים במים מתרחשת עקב דה-פולימריזציה של מולקולת החלבון, המתרחשת, למשל, במהלך המעבר של קולגן לגלוטן.
הידרוליזה חלבון יכול להיגרם באמצעות אנזימים proteolytic המשמשים להגברת תהליכים טכנולוגיים מסוימים (ריכוך בשר קשה, ביצוע בצק שמרים, וכו ').
1.1. חלבונים. חומצות אמינו - מרכיבים מבניים של חלבונים
1.2. מבנה וסיווג של חומצות אמינו
1.3. רמות הארגון המבני של מולקולות חלבון
1.4. תכונות פיסיקליות-כימיות של חלבונים
1.5. סיווג חלבונים
1.6. פחמימות. סיווג פחמימות
1.7. שומנים
1.8. ויטמינים
1.8.1. ויטמינים מסיסים בשומן
1.8.2. מים מסיסים ויטמינים
1.8.3. ויטמין-כמו חומרים.
2.1. אנזימים וזרזים אנאורגניים
2.2. מבנה אנזים
2.3. קואנזימים
2.4. תכונות אנזים
2.5. אנזים המינוח
2.6. סיווג אנזים
2.7. מנגנון הפעולה של אנזימים
2.8. עיכוב פעילות האנזים
3.1. התפקיד הביולוגי של פחמימות
3.2. טרנספורמציה של פחמימות בדרכי העיכול
3.3. ביוסינתזה ופירוק גליקוגן
3.4. דרכים עיקריות לקטבוליזם של גלוקוז
3.4.1. גליקוליזה אנאירובית
3.4.2. גליקוליזה אירובית (מסלול הקסוז-דיפוספט)
3.4.3. מסלול Hexosomonophosphate
3.4.4. גלוקונוגנזה
4.1. השומנים העיקריים של גוף האדם הם התפקיד הביולוגי שלהם.
4.2. עיכול שומנים, רזינתזה שומן
4.3. ליפופרוטאינים בדם
4.4. חמצון של חומצות שומן גבוהות יותר
4.5 חמצון גליצרול
4.6. ביוסינתזה של חומצות שומן גבוהות ברקמות
4.7. כולסטרול
5.1. עיכול חלבון
5.2. חומצת אמינו ריקבון, נטרול של מוצרים רקובים
5.3. מטבוליזם של חומצות אמינו
5.4. דרכים לנטרל את האמוניה
6.1. מולקולות איתות
6.2. הורמונים היפותלמוס
6.3. היפמוזה הורמונים
6.4. הורמון בלוטת התריס בלוטת התריס
6.5. הורמונים של בלוטות התריס
6.6. הורמונים של בלוטות המין
6.7. הורמוני הכליה
6.8. הורמונים הלבלב
1. מבוא לביוכימיה
2. אנזימים
3. חילוף פחמימות
4. מטבוליזם שומנים
5. חילופי חלבון
6. תקנה של חילוף החומרים
7. שאלות הבחינה
1.1. סנאים. חומצות אמינו - המרכיבים המבניים של חלבונים
חלבונים
חלבונים הם תרכובות אורגניות בעלות מולקולות חנקן, המורכבות מחומצות אמינו המקושרות בשרשראות עם קשרי פפטידים ובעלי מבנה מבני מורכב.
אותן חומצות אמינו נמצאות בחלבונים של מבנה ותפקוד שונים. האינדיבידואליות של מולקולות חלבון נקבעת על ידי סדר של חילופין של חומצות אמינו בחלבון.
מאפיינים אופייניים של חלבונים המייחדים אותם מתרכובות אורגניות אחרות של התא:
1. חלבונים הם תרכובות המכילות חנקן, כמו מרכיבים רבים אחרים של התא (חומצות גרעין, כמה שומנים, פחמימות), אך בניגוד לחומרים אורגניים אחרים, תכולת החנקן גבוהה בהרבה - בממוצע 16 גרם ל -100 גרם חלבון.
2. היחידה המבנית של חלבונים הם חומצות אמינו אלפא של L-series.
3. חומצות אמינו כרוכות בחלבונים על ידי קשרים פפטידים, ויצרו שרשרת פוליפפטיד.
4. לחלבונים יש משקל מולקולרי גבוה (מ 20,000 עד כמה מיליוני daltons).
5. חלבונים נבדלים בארגון מבני מורכב (יש להם מבנה ראשוני, משני, שלישוני ורביעוני).
תפקודים שונים של חלבונים:
1. קטליטי. חלבונים רבים הם אנזימים
2. רגולטורית. הורמונים מסוימים הם חלבונים.
3. מבנית. כל המבנים של התא החי הם חלבונים.
4. קולטן. חלבונים הם מרכיב חיוני של הקולטנים, המסוגלים לזהות מולקולות אחרות.
5. תחבורה. הם משנים שומנים, פיגמנטים, הורמונים, חומרים מרפא, תרכובות הידרופובי שונות, וכו '
6. תמיכה. קולגן, חלבונים לעצמות.
7. אנרגטי. חמצון של 1 גרם של חלבון מלווה שחרור של 17.6 kJ של אנרגיה. ביום, 15% מהאנרגיה מיוצר עקב התמוטטות של חלבונים.
8. סתירה. פונקציה זו מבוצעת על ידי חלבונים בשריר - אקטין, מיוזין.
9. גנים רגולציה פונקציה של היסטונים.
10. החיסון. נוגדנים הם חלבונים.
11. Hemostatic. פיברינוגן וחלבוני פלזמה אחרים מעורבים בתהליכי קרישת דם.
חומצות אמינו - רכיבים מבניים של חלבונים
חומצות אמינו - תרכובות הטרו-פונקציונליות. הם נגזרות של חומצות קרבוקסיליות, שבהן אטום המימן במיקום אלפא מוחלף על ידי קבוצת אמינו.
כל חומצות האמינו המרכיבות חלבונים מאופיינות בתכונות הבאות:
א) על פי המיקום של קבוצת האמינו, הם חומצות אמינו (קבוצת האמינו עומדת ליד קבוצת carboxyl).
ב) כולם שייכים לסדרה L, שכן קבוצת האמינו באטום הפחמן האסימטרי (כיראלי) נכתבת משמאל. היוצא מן הכלל הוא גליצין, שאין לו אטום פחמן אסימטרי, שרשרת הצד שלו מיוצגת על ידי אטום מימן.
ג) יש להם את אותו השבר המשותף, והם נבדלים רק במבנה של שרשרת הצד (R), אשר תכונותיו קובעות במידה רבה את התכונות של חומצות האמינו והחלבונים שבהם הם מורכבים. זה ההבדלים צורה, גודל קוטביות המאפשרים חומצות אמינו להיות אלה אבני הבניין כי האבולוציה משתמש כדי לעמוד בדרישות מבנה חלבון מחמירים.
g) בפתרונות בערכי pH נייטרליים, חומצות אמינו-אלפא קיימות בעיקר בצורת מלחים פנימיים. במדיום חומצי חזק, הצורה הקטיונית שוררת, בצורה אלקלינית חזקה, אניוני. (
אורגניזמים שונים רבים נמצאו חומצות אמינו רבות שאינן חלק מהחלבונים (חומצות אמינו שאינן חומצות). עם זאת, כל האורגניזמים הידועים לבניית החלבונים שלהם משתמשים באותן 20 חומצות אמינו, F. Crick קרא להם "עשרים קסום". רק הם מוצפנים על ידי הקוד הגנטי.
ביוכימיה INET
ביוכימיה
הסעיף הבאחלבונים. חומצות אמינו - מרכיבים מבניים של חלבונים
חלבונים הם תרכובות אורגניות בעלות מולקולות חנקן, המורכבות מחומצות אמינו המקושרות בשרשראות עם קשרי פפטידים ובעלי מבנה מבני מורכב.
אותן חומצות אמינו נמצאות בחלבונים של מבנה ותפקוד שונים. האינדיבידואליות של מולקולות חלבון נקבעת על ידי סדר של חילופין של חומצות אמינו בחלבון.
מאפיינים אופייניים של חלבונים המייחדים אותם מתרכובות אורגניות אחרות של התא:
1. חלבונים הם תרכובות המכילות חנקן, כמו מרכיבים רבים אחרים של התא (חומצות גרעין, כמה שומנים, פחמימות), אך בניגוד לחומרים אורגניים אחרים, תכולת החנקן גבוהה בהרבה - ממוצע של 16 גרם ל -100 גרם חלבון.
2. היחידה המבנית של חלבונים הם חומצות אמינו אלפא של L-series.
3. חומצות אמינו כרוכות בחלבונים על ידי קשרים פפטידים, ויצרו שרשרת פוליפפטיד.
4. לחלבונים יש משקל מולקולרי גבוה (מ 20,000 עד כמה מיליוני daltons).
5. חלבונים נבדלים בארגון מבני מורכב (יש להם מבנה ראשוני, משני, שלישוני ורביעוני).
תפקודים שונים של חלבונים:
1. קטליטי. חלבונים רבים הם אנזימים
2. רגולטורית. הורמונים מסוימים הם חלבונים.
3. מבנית. כל המבנים של התא החי הם חלבונים.
4. קולטן. חלבונים הם מרכיב חיוני של הקולטנים, המסוגלים לזהות מולקולות אחרות.
5. תחבורה. הם משנים שומנים, פיגמנטים, הורמונים, חומרים מרפא, תרכובות הידרופובי שונות, וכו '
6. תמיכה. קולגן, חלבונים לעצמות.
7. אנרגטי. חמצון של 1 גרם של חלבון מלווה שחרור של 17.6 kJ של אנרגיה. ביום, 15% מהאנרגיה מיוצר עקב התמוטטות של חלבונים.
8. סתירה. פונקציה זו מבוצעת על ידי חלבונים בשריר - אקטין, מיוזין.
9. גנים רגולציה פונקציה של היסטונים.
10. החיסון. נוגדנים הם חלבונים.
11. Hemostatic. פיברינוגן וחלבוני פלזמה אחרים מעורבים בתהליכי קרישת דם.
חומצות אמינו - רכיבים מבניים של חלבונים
חומצות אמינו - תרכובות הטרו-פונקציונליות. הם נגזרות של חומצות קרבוקסיליות, שבהן אטום המימן במיקום אלפא מוחלף על ידי קבוצת אמינו.
כל חומצות האמינו המרכיבות חלבונים מאופיינות בתכונות הבאות:
א) על פי המיקום של קבוצת האמינו, הם חומצות אמינו (קבוצת האמינו עומדת ליד קבוצת carboxyl).
ב) כולם שייכים לסדרה L, שכן קבוצת האמינו באטום הפחמן האסימטרי (כיראלי) נכתבת משמאל. היוצא מן הכלל הוא גליצין, שאין לו אטום פחמן אסימטרי, שרשרת הצד שלו מיוצגת על ידי אטום מימן.
ג) יש להם את אותו השבר המשותף, והם נבדלים רק במבנה של שרשרת הצד (R), אשר תכונות אשר קובעות במידה רבה את התכונות של חומצות אמינו וחלבונים בהם הם מורכבים. זה ההבדלים צורה, גודל קוטביות המאפשרים חומצות אמינו להיות אלה אבני הבניין כי האבולוציה משתמש כדי לעמוד בדרישות מבנה חלבון מחמירים.
g) בפתרונות בערכי pH נייטרליים, חומצות אמינו-אלפא קיימות בעיקר בצורת מלחים פנימיים. במדיום חומצי חזק, הצורה הקטיונית שוררת, בצורה אלקלינית חזקה, אניוני. (
אורגניזמים שונים רבים נמצאו חומצות אמינו רבות שאינן חלק מהחלבונים (חומצות אמינו שאינן חומצות). עם זאת, כל האורגניזמים הידועים לבניית החלבונים שלהם משתמשים באותן 20 חומצות אמינו, F. Crick קרא להם "עשרים קסום". רק הם מוצפנים על ידי הקוד הגנטי.
מבנה וסיווג של חומצות אמינו
ישנם סיווגים שונים של חומצות אמינו המרכיבות חלבונים, בהתאם לתכונה שבבסיס החלוקה שלהם לקבוצות. אז על ידי הטבע הכימי של הצד שרשרת חומצות אמינו מחולקים aliphatic (acyclic), ארומטי, heterocyclic.
I. אליפטית - חומצות אמינו
1. מונומינומונוקרבון (נייטרלי)
חומצות אמינו אליפטיות המכילות קבוצה תפקודית נוספת בשרשרת הצד.
A) קבוצת הידרוקסיל (חומצות הידרוקסילאמינו)
B) קבוצה carboxyl (monoamino dicarboxylic)
B) קבוצה amide
D) קבוצת אמינו (diaminomonocarboxylic)
Ii. חומצות אמינו ארומטיות III. חומצות אמינו הטרוציקליות
Iv. Iminoacid
קבוצות הידרופיליות (קוטביות) הן הקבוצות: -OH, -SH, -COOH, -NH2, ליבת imidazole. Hydrophilicity היא תכונה של מולקולות או קבוצות שיש להם ... בהקשר זה, כל 20 חומצות אמינו ניתן לחלק את תכונות שרשרת הצד שלהם לתוך ...הידרופובי שאינו קוטבי,
פולאר לא יונית,
פולאר טעונה שלילית,
פולאר חיובי חיובי.
שרשראות הצד של חומצות אמינו אלה מכילים קבוצות לא קוטביות ולא יוניות. מחלקה זו כוללת חומצות אמיניות אליפטיות. גליצין הוא הכי ... חומצות אמינו המכילות קוטב, לא יוניים R- קבוצות.חומצות אמינו של קבוצה זו מכילות קבוצות לא יוניות בשרשרת הצד, שאינן מסוגלות לשחרר או לצרף פרוטון. הקבוצות הצדדיות של חומצות אמינו אלה מתמוססות במים כי הם מכילים קבוצות פונקציונליות קוטביות אשר יוצרים קשרים מימן עם מים. אלה כוללים serine, threonine, המכיל hydroxyl אלכוהול בצד שרשרת, כמו גם גלוטמין, אספרגין, המכיל קבוצות amide. קבוצה זו כוללת גם ציסטאין וטירוזין. חומצות אמינו אלה כוללות בהתאמה קבוצת thiol ו hydroxyl פנולי, מסוגל disociation, אבל על ערכי ה- pH נייטרלי מתוחזק בתאים, קבוצות אלה כמעט לא לנתק.
חומצות אמינו עם קוטב טעונה שלילית
R- קבוצות.
קבוצה זו כוללת חומצות אמינו אספרטיות וגלוטמין, בהן יש קבוצה נוספת של carboxyl המסוגלת לנתק בשרשרת הצד.
חומצות אמינו עם R- קבוצות חיוביות קוטביות חיובי. ליזין יש קבוצה נוספת טעונה חיובי בשרשרת הצד, ... הקודם סעיף רמה עליונה סעיף הבא סעיףרמות הארגון המבני של מולקולות חלבון
המבנה של מולקולות חלבון מאופיין במורכבות ניכרת ובארגון ייחודי. ישנם 4 רמות של ארגון מבניים חלבון: ... המבנה העיקרי הוא רצף חומצות אמינו בשרשרת פוליפפטיד, ... רצף חומצות אמינו בשרשרת פוליפפטיד קובע את רמות הבאים של הארגון המבני חלבון, שלה ...מודולי פרוטאין (תחומים)
חומצה שומן סינתזה, המייצג שרשרת פוליפפטיד אחת, יש 7 תחומים, עבור קטליזה 7 תגובות. ההנחה היא כי תחומים synthase פעם אחת ...המרכז הפעיל של החלבון ואת האינטראקציה שלו עם ליגנד.
הבסיס לתפקודם של חלבונים הוא אינטראקציה ספציפית שלהם עם ligands. 50,000 חלבונים בודדים המכילים פעילות ייחודית ... המבנה הרביעוני הוא הרמה הגבוהה ביותר של ארגון מבניים, אפשרי ... המבנה הרביעוני הוא התייצב על ידי קשרים שאינם קוולנטיים המתעוררים בין רפידות מגע של הפרוטומים, ...תכונות פיסיקליות-כימיות של חלבונים
המבנה העיקרי של חלבונים קובע במידה רבה את המשניים, מבנים שלישוני ותכונות של המבנה הרביעוני. בתורו, המסה המולקולרית של החלבונים היא די גדולה, ולכן הם שייכים ל ... המסה המולקולרית של חלבונים מסוימים היא: אינסולין - 5700D,סיווג חלבונים
גוף האדם מכיל מעל 50,000 חלבונים בודדים, שונים במבנה העיקרי שלהם, קונפורמציה, המבנה של המרכז הפעיל פונקציות. עם זאת, עד כה אין סיווג אחידה קוהרנטית, כי לוקח בחשבון את התכונות השונות של חלבונים. הסיווגים הקיימים מבוססים על מאפיינים שונים. כך ניתן לסווג חלבונים:
· בצורה של מולקולות חלבון (עגול - עגול או fibrillar - filamentary)
לפי משקל מולקולרי (משקל מולקולרי נמוך, משקל מולקולרי גבוה)
· בהתאם לתפקודים המבוצעים (תחבורה, מבניים, מגנים, רגולטוריים וכו ')
· לוקליזציה בתא (גרעיני, cytoplasmic, lysosomal, וכו ')
· על פי המאפיינים המבניים וההרכב הכימי, החלבונים מתחלקים לשתי קבוצות: פשוט ומורכב. חלבונים פשוטים מיוצגים רק על ידי שרשרת פוליפפטידים המורכבת מחומצות אמינו. חלבונים מורכבים מכילים חלק חלבון ומרכיב שאינו חלבון (קבוצה תותבת). עם זאת, סיווג זה אינו אידיאלי, שכן בצורתו הטהורה, חלבונים פשוטים נמצאים לעיתים נדירות בגוף.
מאפיינים של חלבונים פשוטים.
היסטונים - חלבוני רקמות של אורגניזמים רבים המשויכים לדנ"א הכרומטין. אלה הם חלבונים במשקל מולקולרי קטן (11-24,000 YES). על פי ... ישנם 5 סוגים של histones. החלוקה מבוססת על מספר שלטים, העיקריים של ... התפקיד העיקרי של ההיסטונים הוא מבני ורגולציה. הפונקציה המבנית היא כי histones מעורבים ...אלבומין וגלובולינים.
A ו- G חלבונים כי הם בכל הרקמות. סרום הדם הוא העשיר ביותר בחלבונים אלה. התוכן של אלבומין זה 40-45 גרם / ליטר, ... אלבומין חלבונים של משקל מולקולרי נמוך יחסית (15-70000 כן); הם ... בשל hydrophilicity גבוהה שלהם, גודל קטן של מולקולות, ריכוזים משמעותיים של אלבומין לשחק תפקיד חשוב ...פרופלמינים וגלוטלין.
גלוטלינים הם גם חלבונים צמחיים, מסיסים במים, פתרונות של מלחים, ואתנול. הם מסיסים באלקליס חלש.פרוטינואידים.
כל החלבונים הללו הם fibrillar, לא hydrolyzed בדרכי העיכול. קולגן מפצה 25-33% מהכמות הכוללת של חלבון ... אלסטין הוא המרכיב המבני העיקרי של סיבים אלסטיים, אשר ...חלבונים מורכבים
בנוסף לרשתות פוליפפטיד, חלבונים מורכבים מכילים חלק לא חלבון (תותבת) המיוצג על ידי חומרים שונים. בהתאם לאופי הכימי של החלק שאינו חלבון, הקבוצות הבאות של חלבונים מורכבים נבדלות:
· chromoproteins
· פחמימות - קומפלקסים חלבונים
· קומפלקסים של שומנים בדם
· נוקלאופרוטאינים
· פוספופרוטאינים
כרומופרוטין
כרומופרוטינים - אלה חלבונים מורכבים, החלק התותב של מיוצג על ידי רכיב צבעוני (מיוונית, כרומוז - צבע). אלה כוללים חלבונים ביולוגיים חשובים המוגלובין, מיוגלובין, וכן כמה אנזימים: קטליז, פרוקסידאז, ציטוכרומים, הם כולם hemproteins, שכן החלק התותב שלהם מכיל heme.
המוגלובין (HB).
יחידות משנה של HB "מכירים" זה את זה בשל נוכחותם של חלקים משלימים על הצורה על פני השטח שלהם. כל יחידות משנה או פוליפפטיד ... כל אחד protomers המוגלובין הוא תיאום טבעי ...סוגי המוגלובין.
הסוגים הפיזיולוגיים של המוגלובין נבדלים זה מזה על ידי שרשרת של שרשראות פוליפפטיות או יחידות משנה שנוצרו בשלבים שונים של התפתחות ... א) פרימיטיבי NVR, מופיע בשלבים הראשונים של התפתחות העובר (1 - ... ב) המוגלובין HbF עוברית (מן העובר הלטיני - העובר). HBF הוא הסוג העיקרי של המוגלובין העובר והוא ...GLYKOPROTEINY (GP)
פרוטוגליאנס
שרשראות הפחמימות הקצרות של HP בנויות מגלוקוזאמין, גלקטוזמין, גלוקוז וגלקטוז. מונוסכרידים המשמעותי ביותר בהרכב של GP - N - ... מספר שרשראות פחמימות קצרים GP יכול להגיע 300-800. אורך ו ...תפקיד האינטראקציה הסלקטיבית של הכרה ספציפית.
תאים סלולריים הממוקמים על פני השטח של הממברנות מעורבים בתהליכים מתוחכמים מאוד של הכרה ביולוגית ואינטראקציה בין-תאית, הפועלים כמערכות קולטן עבור תרכובות מסוימות ותאים.
תפקיד התחבורה
GP לבצע הובלה של חומרים הידרופובי יונים מתכת. אז
הפונקציה של המוביל של ברזל מתבצעת על ידי GP - transferrin; נחושת - ceruloplasmin; הורמונים סטרואידים - טרנסקורטין.
קטליטי.
מרכיב הפחמימות נמצא בהרכב של כמה אנזימים: enterokinase, peroxidase, oxidase גלוקוז, cholinesterase.
מגן שמן פונקציה.
גליקופרוטאינים הם חומרים מכוננים של הריריות של הרוק, קיבה ומעיים של המעיטים.
להשתתף בתהליך של קרישה דם.
פרוטוגליאנס. אלו הם פחמימות, קומפלקסים חלבונים, מרכיב פחמימות אשר מיוצג על ידי heteropolysaccharides שנבנו מ ...ליפופרוטאינים חופשיים.
ליפופרוטאינים של פלסמה בדם, חלב, מסיסים במים.
פרוטוליפידים מבניים.
הם חלק ביומברנות, מסיסים בשומנים.
מתחמי שומנים בדם מכילים רכיבי שומנים כחלק שאינו חלבון.
חומצות שומן גבוהות יותר
ליפופרוטאינים חופשיים.
LP FRACTIONS: א) Chylomicrons (HM). זהו שבר צפיפות הנמוך ביותר, מאז כחלק מ ... B) צפיפות נמוכה מאוד ליפופרוטאינים (VLDL). או pre-b-lipoproteins, הצפיפות שלהם היא 0.94 - 1.006 kg / l;ליפופרוטאינים מבניים (פרוטאוליפידים).
נוקלופרוטינים
חומצות גרעין הן תרכובות מולקולריות גבוהות המורכבות מונונוקליאוטידים, כלומר. היחידה המבנית שלהם היא mononucleotide ... תרכובת הבסיס pentose נקרא nucleoside, הקשר בין pentose לבין בסיס חנקני (ב הוא glycosidic) ...המינוח של הנוקליאוטידים הנפוצים ביותר.
1. Adenosine monophosphate (AMP), חומצה אדניליק. 2. Guanosine monophosphate (GMP), חומצה guanylic. 3. montosphate cytidin (CMP), חומצה ציטידית.מבנה חומצות גרעין.
במקביל, האג"ח אסתר נוצר על ידי שאריות פוספט של mononucleotide אחד ו 3 "על ידי קבוצת hydroxyl של שאריות pentose של אחר ... הקצוות של polynucleotides שונים במבנה: בקצה אחד יש ...המבנה המשני של הדנ"א.
על פי מודל זה, מולקולת הדנ"א היא סליל כפול שנוצר על ידי שתי רשתות poliucleotide מעוותות זו לזו ... כל הבסיסים של רשתות ה- DNA (הידרופובי של נכסים) ממוקמים בתוך הכפול ... בנוסף קשרים מימן, אינטראקציות הידרופובי המתרחשים הייצוב של המבנה המשני של ה- DNA ...תכונות של המבנה של רנ"א.
המבנה העיקרי של רנ"א בדומה למבנה העיקרי של ה- DNA הוא שרשרת polynucleotide המורכב mononucleotides מחובר על ידי 3 "5" - קשרים phosphodiester.
המבנה המשני של רנ"א.
הסוגים העיקריים של RNA.
1. תחבורה RNA (tRNA) המבנה המרחבי של tRNA, ללא קשר להבדלים ברצף ...מבנה שלישוני של חומצות גרעין.
המחקר של כמה וירוסים דנ"א של המיטוכונדריה, chloroplasts בשיטות פיזיות, פיסיקליות וכימיות הראה כי סליל כפול DNA על ... המבנה סופר סליל (supercoiled) מספק אריזה חסכונית ... הנתונים הזמינים על המבנה של tRNA עולה כי מולקולות tRNA יליד יש בערך אותו ...פוספאופרוטינים.
נקבע כי phosphoproteins בתאים מסונתזים כתוצאה של זרחון עם השתתפות של קינאזות חלבון. Phosphoproteins כוללים חלב caseinogen, שהוא חלבון ...פחמימות. סיווג פחמימות
המונח "פחמימות", שהוצע במאה ה XIX, התבסס על ההנחה שכל הפחמימות מכילות שלושה אלמנטים - פחמן, מימן וחמצן, היחס בין האחרונים כמו במים, והרכב היסודי יכול לבוא לידי ביטוי על ידי הנוסחה Сn (Н 2 О) m. עם זאת, כמו פחמימות חדשות התגלו, הם גילו כי לא כולם מספקים את הנוסחה הזו.
המונח "פחמימות" הוא מיושן ואינו משקף את הטבע הכימי או את הרכב התרכובות הללו, אך המונח "גליצידים" המוצע להם אינו נפוץ.מאפיין ייחודי המאפיין של פחמימות הוא נוכחות של לפחות שתי קבוצות hydroxyl ו carbonyl (אלדהיד או קטון) קבוצות, כלומר פחמימות הן תרכובות polyoxycarbonyl ונגזרותיהן.
פחמימות הן המעמד השכיח ביותר של תרכובות אורגניות בטבע. הפונקציות של פחמימות בתאים הם מגוונים מאוד. הם משמשים כמקור וצובר של אנרגיית התא, ממלאים תפקיד מבניים, הם בצורה של glycosaminoglycans והם חלק מטריקס תאיים, להשתתף בתהליכים מטבוליים רבים.
מונוסכרידים הם פחמימות שאינן הידרוליזה, כלומר. לא להישבר לתוך סוכרים פשוטים. Oligosaccharides הם פחמימות מורכבות המכילות 2-10 monosaccharide שאריות.
סוכרים הם תרכובות מולקולריות גבוהות אשר מקרומולקולות להכיל מאות אלפי שאריות monosaccharide של סוג אחד (homopolysaccharides) או סוגים שונים (הטרופוליסכרידים).
2.2. מונוככרידים
הסיווג של מונוסכרידים מבוסס על שתי תכונות:
נוכחות של קבוצות פונקציונליות.
מספר אטומי הפחמן בהרכב מונוסכרידים.
בהתאם למיקום בקבוצת carbonyl, monosaccharides מחולקים aldoses ו ketoses. Aldoses להכיל קבוצה אלדהיד, ואילו ketoses להכיל קבוצה keto.
בהתאם למספר אטומי הפחמן, הקבוצות הבאות של monosaccharides נבדלים: triose, tetrose, pentose, hexose, heptose
הצורות הפתוחות (הלא סגורות) של מונוסכרידים מתוארות כנוסחאות הקרנת פישר. מולקולות monosaccharide להכיל מספר מרכזי כירליות (C *) ו שייכים תרכובות של L או D סדרה.
התצורה היחסית של מונוסכרידים נקבע על ידי תקן התצורה - גלידה אלדהיד.
מונוסכרידים שייכים לסדרת ה- D אם קבוצת ה- OH באטום פחמן כרום נמוך יותר נמצאת בצד ימין ובסדרת L אם קבוצת OH נמצאת בצד שמאל. לכן, הידרוקסיל עומד באטום כיראלי התחתונה נקרא D-, L- קביעת.
ב תמיסה מימית הן צורות פתוחות מחזורית של monosaccharides. צורות מחזוריות של חמישה חברים (furanose) ו שש חברות (pyranose) heterocycles.
שמות המחזורים נובעים משמות של תרכובות קשורות - פוראן ופיראן.
הצורות המעגליות של מונוסכרידים הן חצי-אצטליות. הם נוצרים עקב האינטראקציה intramolecular בין קבוצות carbonyl ו hydroxyl של monosaccharide. בצורת מחזורית, מרכז חדש של chirality מתעוררת, כמו גם הידרוקסיל חדש - חצי cytal. זה מוביל להיווצרות של זוג אחר של איזומרים, אשר נקראים אנומרים.
עבור צורות מחזוריות של מונוסכרידים, נוסחאות Hewors מבטיח הם אימצו, שבו המחזורים מתוארים כמו פוליגונים שטוח שוכב בניצב אל המטוס של הדמות. אטום החמצן ממוקם במעגל pyranose בפינה הימנית הרחוקה, ב furanous - מאחורי המטוס של המחזור. סמלים של אטומי פחמן במחזורים אינם נכתבים.
כדי לעבור מ נוסחאות ההקרנה של פישר לנוסחאות של היורס, יש לזכור את הדברים הבאים: אטומים וקבוצות של אטומים הממוקמים בנוסחאות פישר משמאל לשרשרת הפחמן, בנוסחאות Hewors נמצאים מעל המטוס של המחזור; תחליפים ממוקמים מימין - מתחת למטוס.
בהתחשב האמור לעיל, monosaccharides החשובים ביותר נוסחאות Heurs הם כדלקמן.
מונוסקצרידים נגזרים
Sialic חומצות בעיקר לקבוע את האינטראקציה של ליגנד עם receptors ...אוליגוסכרידים
לקטוז ו maltose שייכים disaccharide הפחתת. הקשר הגליקוזידי בתוכם נוצר על ידי הקבוצה OH hemiacetal (glycosidic) ... בניגוד maltose ולקטוז, סוכרוז הוא ללא הפחתת ... מלטוז (סוכר מלט) נוצר על ידי התמוטטות של עמילן במעי. מוכלה כמויות גדולות מלט ...הומופולסקרידים (PS).
- המבנה של monosaccharides המהווים את השרשרת - סוג של קשרים גליקוזידים חיבור מונומרים לתוך השרשרת - רצף של שאריות monosaccharide בשרשרת.הטרופוליס
גליקנים גליקוזיים הם שרשראות ארוכות ובלתי מסודרות של הטרופוליסכרידים שנבנו ביחידות דיסכרידיות חוזרות - דימרים ... הגליקנים העיקריים של הגליקוזמין הם: חומצה היאלורונית, ... חומצה היאלורונית בנויה מיחידות חוזרות, כולל חומצה גלוקורונית ו- N-acetylglucosamine.שומנים
שומנים
המונח "LIPIDS" מאחד חומרים עם תכונה פיזית משותפת - הידרופוביות, כלומר. מסיס במים. לפי מבנה, שומנים הם תרכובות של מבנה כימי שונה. הם מחולקים לשיעורים, בהם הם משלבים מולקולות בעלות מבנה כימי דומה ותכונות ביולוגיות שכיחות.
עיקר השומנים בגוף הם שומנים - triacylglycerols, שהם צורה של אנרגיה בתצהיר.
פוספוליפידים הם סוג גדול של שומנים המכילים חומצה חומצה זרחתית, נותן להם תכונות amphiphilic. בשל תכונה זו, phospholipids טופס מבנה bilayer קרום שבו חלבונים שקועים.
סטרואידים, המיוצגים בעולם החי על ידי כולסטרול ונגזרותיו, מבצעים פונקציות שונות.
חומצות שומן ואסילגליצרול.
חומצות שומן הן מרכיבים מבניים של שומנים שונים. חומצות שומן בדם האדם הם שרשרת פחמימנים לא מסודרים על ... קשרים כפולים בחומצות שומן בגוף האדם יש את תצורת CIS. חומצות רוויותפוספוליפידים וספינגוליפידים
פוספוליפידים
Glycerophospholipids הם נגזרות של גליצרול, שבו אטומים פחמן הראשון והשני מקושרים על ידי האג"ח אסטר מורכבות כדי שאריות חומצות שומן, ... כמות קטנה, אבל מוצר ביניים בדרך של סינתזה ... ב גליצריופוליפידים, אטום פחמן הראשון של גליצרול הוא esterified עם חומצות שומן רווי, השני ...ספינגוליפידים
כל אלה הם spingosine קשורה חומצות שומן יוצא דופן (amide הקשר), וקבוצות hydroxyl מסוגלים לתקשר עם אחרים ... Sphingomyelins N הם נגזרות של acyl של sphingosine, קבוצת אמינו שבו ... בתא, sphingomyelins הם המרכיבים העיקריים של המיאלין ואת תאי המוח ואת רקמת העצבים. חלק פתולוגי ...סטרואידים
כולסטרול יכול להיות esterified ידי קבוצה hydroxyl עם חומצות שומן, ויצרו אסתר של כולסטרול. ב טופס לא esterified, כולסטרול הוא חלק מממברנות של תאים שונים.ויטמינים
באמצע המאה ה -19, הערך התזונתי של חלבונים, שומנים, פחמימות, מינרלים ומים התפתחו. עם זאת, ניסיוני ... בשנת 1880 N.I. Lunin ניהל מחקר עם עכברים, קבוצה אחת של עכברים ... רופאים ביפן ואינדונזיה ציינו בפועל שלהם כי חולים אשר משתמשים בעיקר אורז מלוטש לעתים קרובות יותר ...דיאטה למבוגרים
בפיתוח של אספקה לקויה של ויטמינים, השימוש הנוכחי של מוצרי מזון נתון ... משחק תפקיד מסוים.לכן, דיאטה קלוריה של אדם מודרני לא ...ויטמינים מסיסים בשומן
ויטמין A הוא שם כימי - retinol, השם הקליני הוא נגד xerophthalmic. רטינול מורכב טבעת בטא יון שרשרת בצד ... מוצרים, ויטמין A ניתן למצוא בצורה של אסטרים palmitate retinyl, ... ההשפעות הביולוגיות של ויטמין A.מים מסיסים ויטמינים
ויטמין C. השם הקליני של ויטמין זה הוא antiscorbutic, ואת השם הכימי ...ויטמין-כמו חומרים.
PABK (PARAMAINOBENZOOIC K-TA) 1.Participates במבנה של חומצה FOLYEVOYA, 2.Participates במבנה של מספר אנזימים,אנזימים וזרזים אנאורגניים
אנזימים הם זרזים ביולוגיים בעלי אופי חלבון. תפקידם של האנזימים בגוף הוא עצום. בכל תא של הגוף הוא עד ... תכונות כלליות של אנזימים וקליסטונים לא ביולוגיים.מבנה אנזים
אנזימים פשוטים מיוצגים רק על ידי החלק חלבון (המורכב מחומצות אמינו) - pepsin, טריפסין, phosphatase. אנזימים מורכבים מיוצגים על ידי: 1. חלק החלבון (המורכב מחומצות אמינו) הוא אפואנזים;איור. מרכז אנזים פעיל
קואנזימים
קואנזימים הם חלק לא חלבון של אנזימים מורכבים. הם מחולקים לשתי קבוצות: 1. ויטמין. 2. Nevitaminnye.תכונות אנזים
1. פעילות קטליטית גבוהה. 2. אנזימים, להיות חלבונים, התערוכה תכונות thermolabile - ... כאשר הטמפרטורה עולה כל 10 מעלות צלזיוס, את המהירות של תגובות אנזימטיות מגדילה 1.5-2 פעמים ...הספציפיות של פעולת האנזימים.
1. ספציפיות מוחלטת. יש אנזימים שפועלים רק על מצע אחד ולא פועלים על מצעים אחרים. Urease מזרז את הידרוליזה של אוריאה.אנזים המינוח
1. מינוח טריוויאלי. דוגמה: pepsin, טריפסין. 2. עבודה המינוח: שם S + סוג של טרנספורמציה + סיום "ase".סיווג אנזים
סיווג אנזים
הבסיס הוא סוג של תגובה קטליזד
חוגים אנזים
חמצון חמצון
העברה
הידרולים
ליאז
Isomerase
סינתיטאז
מנגנון הפעולה של אנזימים
שלב 1 מאופיין על ידי דיפוזיה של המצע לאנזים ואת האינטראקציה הסטרית שלהם עם היווצרות של תסביך המצע האנזים. שלב זה ... Е + S\u003e ЕSבשלב השני, טרנספורמציה של מורכבות E-S לתוך אחד, או כמה, מתחמי מופעל מתרחשת.
Е + S\u003e ЕS\u003e ЕS *\u003e ЕS **\u003e ЕР
שלב זה הוא הארוך ביותר בזמן. כאשר זה קורה, שבירת קשרים במולקולה המצע מתרחשת, היווצרות של אג"ח חדשות, כלומר. מוצרי התגובה נוצרים. אנרגיית ההפעלה יורדת באופן משמעותי.
בשלב השלישי, מוצרי התגובה משוחררים מן האנזים ומשוחררים לסביבה.
EP\u003e E + P
האצת התגובה הכימית על ידי אנזימים מתרחשת עקב ירידה משמעותית באנרגיית ההפעלה של החומרים המגיבים. מספר תופעות מולקולריות יכול להפחית את האנרגיה ההפעלה.
השפעות מולקולריות
השפעת הריכוז.
מולקולות התת-קרקע מרוכזות באזור המרכז הפעיל של האנזים.
השפעת ההתכנסות והכיוון.
זהו מאפיין אופייני של אנזימים, אשר מאפשר לך להאיץ את השינוי של המצע ולהגדיל את קצב התגובה של 1000 ו 10,000 פעמים. אתרי הקשר של המרכז הפעיל של האנזים נקשרים במיוחד למולקולות המצע, מביאים אותם יחד ומספקים אוריינטציה הדדית, כך שהיא מועילה לפעולתן של הקבוצות הקטליטיות של האנזים. סידור מסודר כזה של המצע מוביל לירידה באנרגיית ההפעלה.
השפעת המתח.
לפני חיבור המצע למרכז הפעיל של האנזים, המולקולה שלו נמצאת במצב רגוע. לאחר מחייב, המולקולה המצע מתמתח ולוקח על תצורה מעוותת מתוח. יחד עם זאת, אורך האג"ח הבין-אטומי גדל, ולכן, האנרגיה ההפעלה פוחתת.
חומצה בסיס קטליזה.
קטליזה קוולנטית.
הוא נצפה באנזימים היוצרים קשרים קוולנטיים בין הקבוצות הקטליטיות של המרכז הפעיל לבין המצע. כתוצאה מכך, מורכב ביניים אנזים המצע מורכב, אשר אינו יציב, מפורקת בקלות, מוצרי התגובה משוחררים במהירות.
השפעת תאימות המושרה.
הוא מסביר את הספציפיות של פעולת האנזימים. בהזדמנות זו, יש 2 נקודות מבט:
א) השערתו של פישר.
ב). התיאוריה של המכתב המושרה של קושלנד הוסיף את התיאוריה של פישר. לדבריה, מולקולת האנזים אינה מבנה קשיח, אלא גמיש. לאחר ... סעיף הקודם סעיף ברמה עליונה ...- זוהי ירידה בפעילות הקטליטית בנוכחות חומרים מסוימים - מעכבים.

לפי אופי הפעולה, מעכבי מחולקים 2 קבוצות גדולות:
Reversible - אלה הם compounds כי אינטראקציה UNQOVALENTLY עם האנזים, ובכך להרכיב מורכבת מסוגל disociation.
בלתי הפיך - אלה הם תרכובות שיכולים לקשור ספציפיות קבוצות תפקודיות מסוימות של המרכז הפעיל של האנזים. הם יוצרים איתו קשרים קוולנטיים חזקים, ולכן זה מורכב קשה להרוס.
סוגי עיכוב.
על פי מנגנון הפעולה, מובחנים סוגי המעצרים הבאים:
עיכוב תחרותי הוא עיכוב התגובה האנזימטית הנגרמת על ידי קשירה למרכז הפעיל של אנזים המעכב, אשר במבנה שלו קרוב למבנה המצע. במקרה זה, הן המצע והן המעכב יכולים לקיים אינטראקציה עם האנזים, אך הם יתחרו על המרכז הפעיל של האנזים, והחומר הגדול יותר יקושר.
לדוגמה:
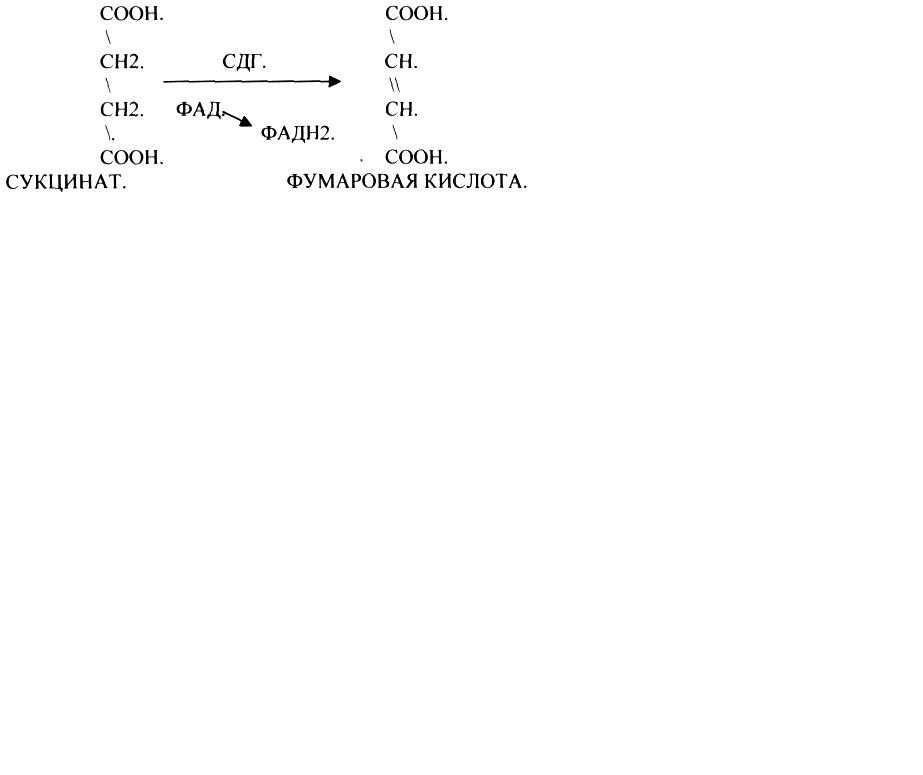
תגובה suhyinate dehydrogenase.
חומצה Malonic הוא מעכב תחרותי של תגובה זו, ולכן, הן חומצה נקשר למרכז פעיל של האנזים, בהתאם היחס שלהם פתרון. כדי להסיר חלקית או לחלוטין את הפעולה של מעכב תחרותי, יש צורך להגדיל את הריכוז של המצע. במקרה זה, האנזים כולו יהיה בצורה של תסביך אנזים-תרכובת, ושיעור המעבד האנזים-מעכב יקטן בחדות, ולכן קצב התגובה האנזימטית עשוי להיות מקסימלי אפילו בנוכחות מעכב.
תרופות רבות לפעול כמו מעכב תחרותי. יחד עם זאת, הם מעכבים את הפעילות של מספר אנזימים הדרושים לתפקוד של תאים חיידקיים. דוגמה לכך היא השימוש של sulfonamides. עבור מחלות זיהומיות שונות הנגרמות על ידי חיידקים, תרופות sulfa משמשים.
תרופות אלו הן דומות מבחינה מבנית לחומצה פרה-אמינובנצויקית, המשמשת את החיידקים לסינתזה של חומצה פולית, הנחוצה לצמיחה ולשגשוג של חיידקים.
המבוא של sulfonamides מוביל עיכוב של אנזימים של חיידקים לסנתז חומצה פולית. הפרת הסינתזה של חומצה זו מובילה להפרת הצמיחה של מיקרואורגניזמים ומוות שלהם.
על פי העיקרון של מעכבי התחרות, יש קבוצה שלמה של תרופות שונות - אלה anticholinesterase. הם מעכבי תחרותי של אנזימים cholinesterase כי מזרז את הידרוליזה של אצטילכולין. אצטילכולין מספק דחף עצבי. Anticholinesterase מתחרה עם אצטילכולין עבור האתר הפעיל של האנזים cholinesterase. כתוצאה מכך, ריקבון של אצטילכולין הוא מעוכב, הוא מצטבר בגוף, גרימת הפרה של הדחפים העצביים.
עיכוב לא תחרותי הוא עיכוב של התגובה האנזימטית שנגרמת על ידי השפעת המעכב על המרה קטליטי של המצע. במקרה זה, מעכב אינו משפיע על הכריכה של האנזים על המצע. מעכב לא תחרותי יכול להיקשר לקבוצות הקטליטיות של המרכז הפעיל של האנזים, או מחוץ למרכז הפעיל של האנזים, אך הוא משנה את הקונפורמציה של האנזים ומשפיע על האתר הקטליטי של המרכז הפעיל שלו. עם עיכוב לא תחרותי, היווצרות של משולש משולש לא פעיל אפשרי.

תכנית עיכוב לא תחרותית
ציאנידים פועלים כמעכבים לא תחרותיים. הם קשורים חזק עם יונים ברזל, שהם חלק האנזים heatal קטליטי, ציטוכרום אוקסידאז. אנזים זה הוא אחד המרכיבים של שרשרת הנשימה. חסימת שרשרת הנשימה מכבה אותו מהעבודה, מה שמוביל למוות מיידי של הגוף.
דוגמה למעכב לא תחרותי היא פעולת מלחי מתכת כבדים. הם חוסמים את קבוצות ה- SH הנכנסות אל האתר הקטליטי של האנזים. זה יוצר מעכב אנזים מורכב. הוא מסוגל לצרף את המצע, אבל שינוי נוסף של המצע אינו מתרחש, כי קבוצות אנליטיות קטליטיות חסומות. התגובה היא לא פרודוקטיבית. כדי להסיר את ההשפעה של מעכב לא תחרותי קשה מאוד, כי יונים מתכת קשורים מאוד מאוד עם המרכז הפעיל של האנזים. פעולתו של מעכב זה ניתנת להסרה רק בעזרת חומרים מיוחדים - רטיוורטורים.
3. מעכב התשתית הוא עיכוב של התגובה האנזימטית הנגרמת על ידי עודף של המצע. נוצר תסביך אנזים-תרכובת, אך הוא אינו עובר שינויים קטליטיים, שכן עושה את מולקולת האנזים לא פעילה. הפעולה של מעכב המצע מוסרת על ידי הקטנת הריכוז של המצע.
4. עיכוב אלוסטרי מאפיין של אנזימים בעל מבנה quaternary, מולקולה אשר מורכב של מספר יחידות (protomers). אנזימים אלוסטריים עשויים להיות 2 יחידות או יותר. במקרה זה, לאחד יש מרכז קטליטי והוא נקרא קטליטי, והשני הוא מרכז אלוסטרי, והוא נקרא אחד הרגולציה. בהיעדר מעכב אלוסטרי, המצע מחובר למרכז הקטליטי, והתגובה הרגילה של הקטליטיזם מתנהלת. כאשר מעכב אלוסטרי מופיע, הוא מצטרף ליחידה הרגולטורית, כלומר. אל המרכז האלסטרי, ומשנה את הקונפורמציה של מרכז האנזים, וכתוצאה מכך פעילות האנזים יורדת.
פחמימות
1. הפחמימות הבסיסיות של האורגניזם החי, תפקידן הביולוגי. 2. טרנספורמציה של פחמימות באיברים של מערכת העיכול. 3. ביוסינתזה ופירוק של גליקוגן ברקמות.התפקיד הביולוגי של פחמימות
1. אנרגיה. במהלך החמצון של 1 גרם של פחמימות למוצרים הסופי (CO2 ו H2O) הוא שוחרר ... 2. מבנית.טרנספורמציה של פחמימות בדרכי העיכול
DIGESTIVE TRACT הפחמימות העיקריות של מזון עבור גוף האדם הם: עמילן, גליקוגן, ... עמילן מזון (גליקוגן) בחלל הפה עובר הידרוליזה על ידי פעולה של רוק אלפא עמילאז, ...ביוסינתזה ופירוק גליקוגן
מחלות גליקוגן. נמצא כי גליקוגן יכול להיות מסונתז כמעט בכל ...גליקוליזה אנאירובית
1. בתנאים אנאירוביים 2. בתנאי מזגן וחלל. ANAEROBIC GLYCOLYSIS (GLYCOGENOLYSIS) מתרחשת בציטופלסמה של תאים. חמצון גלוקוז או גלוקוז שאריות גליקוגן ...איור. התמוטטות אירובית של גלוקוז
גליקוליזה אירובית (מסלול הקסוז-דיפוספט)
זוהי הדרך הקלאסית של קטבוליזם פחמימות אירובית ברקמות המתרחשת בציטופלסמה לשלב של היווצרות pyruvate ומסתיים במיטוכונדריה עם ... כאשר החמצן מתחיל להיכנס לתאים, דיכוי אנאירובית מתרחשת ... 1. GlYCERALDEHYDE-3-PHOSPHATEאיור. התמוטטות אירובית של גלוקוז
מסלול Hexosomonophosphate
בתוך רקמות, תגובה כימי. החמצון של גלוקוז לאורך נתיב זה ממשיך בציטופלסמה של התאים והוא מוצג ... התפקיד הביולוגי של מסלול זה של חמצון גלוקוז קשורה בעיקר עם ייצור של שני חומרים:גלוקונוגנזה
המקורות העיקריים של גלוקוז עבור גוף האדם הם: 1. פחמימות מזון; 2. רקמת גליקוגן;השומנים העיקריים של גוף האדם הם התפקיד הביולוגי שלהם.
LIPIDS הם מזון בסיסי. הם נכנסים לגוף האדם במוצרים של צמחים ובעלי חיים. Per diem ... בגוף האדם, LIPIDS מיוצגים על ידי: 1. שומנים מבניים (כולסטרול, פוספוליפידים, גליקוליפידים).עיכול שומנים, רזינתזה שומן
LIPIDS מגיע מזון בפה כפופים רק עיבוד מכני. אנזימים LIPOLYTIC בחלל הפה אינם נוצרים ... 1. נוכחות של חומצות מרה. 2. נוכחות של אנזימים.ליפופרוטאינים בדם
על פי המבנה שלה, micelles LIPOPROTEIN יש שכבה חיצונית הליבה. השכבה החיצונית נוצרת החלבונים, phospholipids וכולסטרול, אשר יש ... ישנם 4 סוגים של LIPOPROTEINS דם, אשר נבדלים זה מזה ... 1. CHILOMICRONES. נוצרו בקיר המעי ויש להם את גודל החלקיקים הגדול ביותר.חמצון של חומצות שומן גבוהות יותר
בתאי רקמת השומן עם השתתפות של lipases, הפירוק של TAG מתרחשת. ליפאז הוא במצב לא פעיל, הוא מופעל על ידי הורמונים (אדרנלין, ... חומצות שומן גבוהות עם אלבומין מועברים בדם לתאי רקמות, איברים, שם ... חמצון של חומצות שומן גבוהות.חמצון גליצרול
החמצון של גליצרול ברקמות קשורה קשר הדוק GlYCOLYSIS, שבו מטבוליטים גליצרול מעורבים כדלקמן:
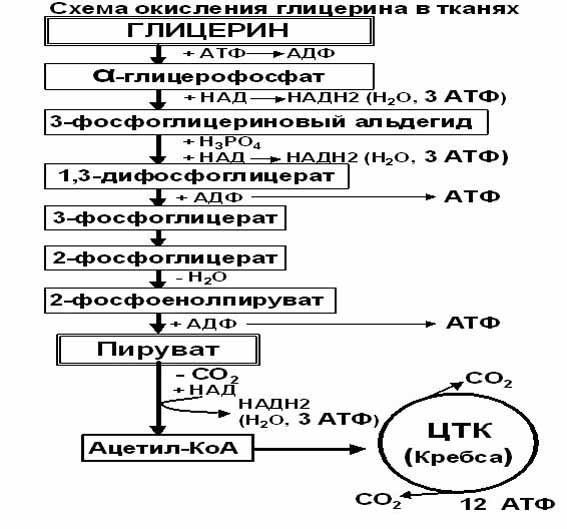
החמצון של גליצרול יצרו את המוצרים הסופיים:
CO2 בשלב הטרנספורמציה:
PIRUVATA
Isocitrate
אלפא-קטוגלוטראט
H 2 אודות שלב השינוי:
Alpha-glycerophosphate
גליקרלדהיד-3-פוספט
פוספלוגרפיה
PIRUVATA
Isocitrate
אלפא-קטוגלוטראט
סוציאציה
מלטה
ATP פרסמה עקב תגובות
א) זירעון התשתית בשלבי השינוי:
Diphosphoglycerate
Phosphoenolpyvate
Succinyl CoA
ב) זרחון חמצוני בשלבי השינוי:
אלפא glyceraphosphate
Glyceraldehyde-3 פוספט
Pyrovate
Isocitrate
אלפא-קטוגלוטראט
סוציאציה
Malate
ההשפעה הכוללת של האנרגיה של חמצון של מולקולת גליצרין אחת הוא 22 ATP.
ביוסינתזה של חומצות שומן גבוהות ברקמות
התנאים עבור biosynthesis של חומצות שומן גבוהות הן: 1. נוכחות של ACETHYL-COA, ATP, CO2, H2O, NADP * H2, 2. נוכחות של חלבונים מיוחדים הספק (HS-APB). 3. נוכחות של אנזימים של סינתזה.כולסטרול
כולסטרול הוא מבשר בסינתזה של סטרואידים: חומצות מרה, הורמונים סטרואידים, ויטמין D3 ... כולסטרול חיוני ...עיכול חלבון
חלבונים למזון עוברים פירוק הידראוליטי תחת פעולת האנזימים הפרוטאוליטיים (מחלקה - הידרולזות, תת - פפטידים). רוב האנזימים האלה מיוצרים בצורה לא פעילה, כלומר. בצורה של ... אנזימים מיוצרים בתאי הקרום הרירי של הבטן או מעיים, תאים הלבלב ו ...חומצת אמינו ריקבון, נטרול של מוצרים רקובים
חומצות אמינו, אשר לא היו נתונים לספיגה, נכנסו למעי הגס, שם הם נרקבים. נרקב של חומצות אמינו הוא תהליך של ריקבון ... תגובה DECARBOXYLATION:מטבוליזם של חומצות אמינו
מקורות חומצות אמינו בתא הם: 1. חלבונים מזון לאחר הידרוליזה שלהם באברי העיכול; 2. סינתזה של חומצות אמינו להחלפה;איור. חימצון חמצוני של חומצה גלוטמית
זיהום עקיף
חומצות האמינו הנותרות עוברים סוג זה של דימינציה, אך באמצעות שלב של טרנזינציה עם חומצה אלפא-קטוגלוטית. אז חומצה גלוטמית (תוצר של תגובה זו) חשוף deamination חמצון.
דרכים לנטרל את האמוניה
אמוניה נוצרת ברקמות שונות. הריכוז בדם אינו משמעותי, שכן הוא חומר רעיל (0.4-0.7 מ"ג / ליטר). ללא שם: במיוחד ... דרכים של מים.איור. גלוטמין
גלוטמין ואספרגין הם חומרים לא רעילים. הם נקראים צורה התחבורה של אמוניה בגוף. הם אינם חודרים לממברנות ובכליות נשברות לחומצות אמינו ולאמוניה.
2. amination Reduction של חומצה אלפא - ketoglutaric
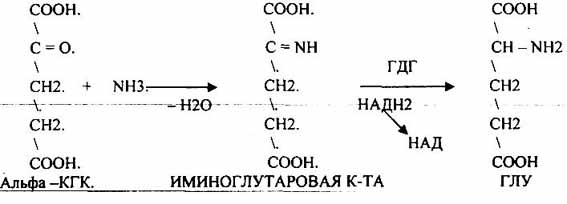
3. היווצרות מלח אמוניום
4. סינתזת אוריאה - הדרך העיקרית של ניטרול אמוניה היא מחזור אורניטין.
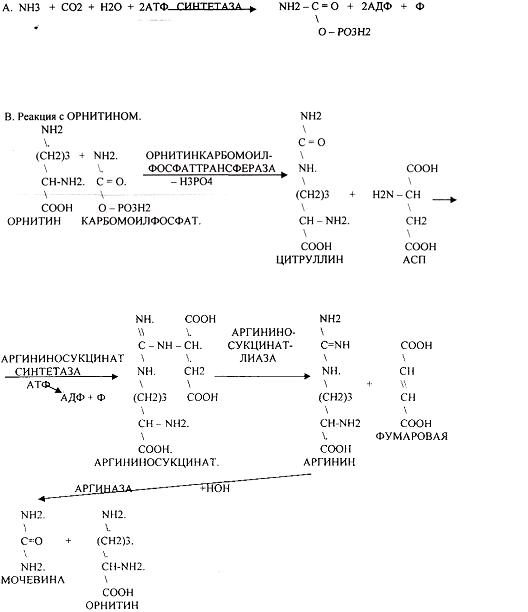
ARGINASE יש ספציפיות מוחלטת והוא נמצא רק בכבד. הרכב של אוריאה מכיל שני אטומי חנקן: אחד בא אמוניה, והשני נגזר TSA.
היווצרות האוריאה מתרחשת רק בכבד.
שתי התגובות הראשונות של מחזור (היווצרות של cytrulline ו arginous succinate) להתרחש המיטוכונדריה, את שאר הציטופלסמה.
הגוף מייצר 25 גרם של אוריאה ליום. אינדיקטור זה מאפיין את תפקוד האוריאה של הכבד. אוריאה מהכבד נכנס לכליות, שם הוא מופרש מהגוף, כמוצר הסופי של חילוף החומרים של חנקן.
- 6.1. מולקולות איתות
- 6.2. הורמונים היפותלמוס
- 6.3. היפמוזה הורמונים
- 6.4. הורמון בלוטת התריס בלוטת התריס
- 6.5. הורמונים של בלוטות התריס
- 6.6. הורמונים של בלוטות המין
- 6.7. הורמוני הכליה
- 6.8. הורמונים הלבלב
חילוף החומרים
המטרות העיקריות של תקנה של מטבוליזם פונקציות הסלולר: 1. תאיים תאיים תאיים של תהליכים מטבוליים; 2. חיסול מחזורים "סרקים" של מטבוליזם, שמוצריהם אינם מבוקשים;מולקולות איתות
הורמונים היפותלמוס
HYPOTALAMUS הוא מרכיב וסוג של "ערוץ פלט" של המערכת הלימבית. זהו קטע של diencephalon השולט פרמטרים שונים ... מצד אחד, הוא מחובר למערכת העצבים המרכזית, מאידך - לבלוטת יותרת המוח דרך אקסונים של הנוירונים ואת המערכת ...היפמוזה הורמונים
היפמוזה הורמונים
ב בלוטת יותרת המוח, האונות הקדמיות (adenohypophysis) והאחוריים (neurohypophysis) מבודדים.הורמון בלוטת התריס בלוטת התריס
הורמון בלוטת התריס בלוטת התריס
בלוטת התריס, הורמונים מסונתזים כי הם נגזרות iodized של טירוזין (ידותירונינים). אלה כוללים triiodothyronine (3, 5, 3? - triiodothyronine, T 3) ו תירוקסין (3, 5, 3 ?, 5, - tetraiodothyronine, T 4).
איור. יודטירונין
ביוסינתזה של יודאת'ירונינים
יודיזציה של טירוזין ויצירת יודיתירונינים מתבצעת בכמה שלבים: 1. הובלת יוד לתאי בלוטת התריס; 2. חמצון של יוד;השפעה על תהליכים מטבוליים
חילופי חלבון
בריכוז פיזיולוגי, יודיתירונינים משפרים את הביוסינתזה של החלבון, אך השפעתם הקטבולית על סינתזת החלבון מתבטאת בריכוז גבוה.
פחמימות
בכבד, בהשפעת ההורמונים הללו, עלייה בשיעור הפירוק של גלוקוז, מתרחשת גליקוגן.
מטבוליזם שומנים
תחת השפעת הורמונים של בלוטת התריס, יש עלייה בפעילות של + Na, K + - ATP, אשר מוביל לירידה ב- ATP בתא, וכתוצאה מכך, כדי ... בריכוזים רגילים, יודיתירונינים לעורר תהליכי צמיחה תא ...הפרעות בהפרשת הורמון בלוטת התריס
Hyposecurity
אצל מבוגרים, ביטוי חמור של חסר הורמון בלוטת התריס הוא myxedema. במקרה זה, ריקבון מאט ... היפותירואידיזם יכול להתרחש גם עקב צריכת יוד לא מספיק ...הפרעת קשב
הורמונים של בלוטות התריס
הורמונים של בלוטות התריס
קולטני PTH ממוקמים על פני השטח של תאי הכליה ורקמת העצם (אוסטאובלסטים, אוסטאוסטיות). מנגנון הפעולה תלוי ב- CAMP. ההשפעות של ההורמון נועדו להגדיל את הריכוז של יוני סידן והפחתת ריכוז של פוספט בדם.מה נעשה עם החומר המתקבל:
אם חומר זה היה שימושי עבורך, תוכל לשמור אותו בדף שלך ברשתות חברתיות: